题目内容
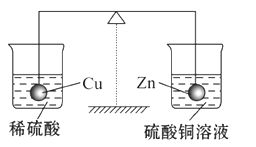
如图,在杠杆的两端分别挂着质量相等的铜球和锌球,这时杠杆平衡。然后将两球分别浸没在稀硫酸和CuSO4溶液中片刻,下列说法中正确的是( )

| A.只有左边烧杯中溶液的质量增加 |
| B.只有右边烧杯中溶液的质量增加 |
| C.两边烧杯中溶液的质量都增加 |
| D.去掉烧杯后,杠杆仍然保持平衡 |
B
铜与稀硫酸不发生反应,所以溶液的质量不发生变化,故A、C错;锌与硫酸铜发生如下反应:Zn+CuSO4=Cu+ZnSO4,由Zn、Cu的相对原子质量可以看出,溶液质量增加,固体质量减少,去掉烧杯后,杠杆左边重,右边轻,故B正确,D错误。

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目