题目内容
已知在通常情况下,过氧化氢| 二氧化锰 |
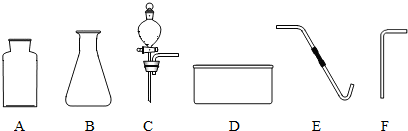
(1)第1套:选用仪器(填选项):
(2)第2套:选用仪器(填选项):
分析:(1)因为通常情况下,过氧化氢
水+氧气,且反应迅速,要利用仪器控制反应速度;
(2)又因为过氧化氢制取氧气符合:固体+液体反应,不需加热;根据氧气的性质,①即:密度比空气的密度大,决定收集方式,用向上排空气法;②氧气难溶于水,也可用排水法.
| 二氧化锰 |
(2)又因为过氧化氢制取氧气符合:固体+液体反应,不需加热;根据氧气的性质,①即:密度比空气的密度大,决定收集方式,用向上排空气法;②氧气难溶于水,也可用排水法.
解答:解:由图可知,排水法要用有橡胶管的导管,便于操作;而排空气法则需要弯玻璃管便可.
故答案为:(1)A、B、C、D、E;(2)A、B、C、F
故答案为:(1)A、B、C、D、E;(2)A、B、C、F
点评:根据制取氧气的反应物和氧气的性质,组装反应及收集装置.

练习册系列答案
相关题目
某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是: .
(2)简述强调“测得的pH小于7”的理由: .
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应.
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了.该小组对这种意外现象的原因作了如下猜想:①可能是酚酞溶液与空气中的氧气反应,使红色消失;②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液.实验中“加热”和“滴入植物油”目的是 .实验结果表明酚酞溶液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:结论1:说明Na2CO3溶液呈 性;结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的NaOH溶液浓度过大:①实验方法 ,②观察到的现象 .
方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.
该组同学将不同浓度的盐酸和NaOH溶液各10mL混合,用温
度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如表).
(1)表中x= .
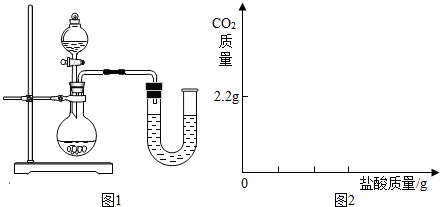
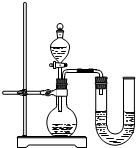
(2)某同学在没使用温度计的情况下,通过右图所示装置完成了实验.则该同学根据 判断NaOH溶液与稀盐酸发生了中和反应.
(3)关于实验中的细节和意外情况:①实验中,稀盐酸必须用胶头滴管逐滴滴加,这样做的目的是 .②实验过程中,要用玻璃棒不断搅拌,这样做的目的是 .③在实验过程中意外发现有气泡出现,你认为原因是 .④发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;你认为:②可能是 ; ③可能是 .
(4)为了进一步研究实验中出现的问题,取了13.3g氢氧化钠固体样品加适量的水配成溶液,向其中加入200g10%的稀盐酸,使其充分反应,生成二氧化碳2.2g.求:
(1)样品中氢氧化钠的质量;
(2)和氢氧化钠反应的盐酸的质量;
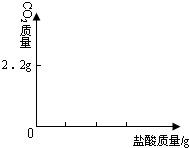
(3)在图中画出以纵坐标表示二氧化碳质量,横坐标表示盐酸的质量的关系图.
(已知Na2CO3+2HCl═2NaCl+H2O+CO2↑)
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:
(2)简述强调“测得的pH小于7”的理由:
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应.
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了.该小组对这种意外现象的原因作了如下猜想:①可能是酚酞溶液与空气中的氧气反应,使红色消失;②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液.实验中“加热”和“滴入植物油”目的是
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:结论1:说明Na2CO3溶液呈
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的NaOH溶液浓度过大:①实验方法
方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.
该组同学将不同浓度的盐酸和NaOH溶液各10mL混合,用温
度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |

(1)表中x=
(2)某同学在没使用温度计的情况下,通过右图所示装置完成了实验.则该同学根据
(3)关于实验中的细节和意外情况:①实验中,稀盐酸必须用胶头滴管逐滴滴加,这样做的目的是
(4)为了进一步研究实验中出现的问题,取了13.3g氢氧化钠固体样品加适量的水配成溶液,向其中加入200g10%的稀盐酸,使其充分反应,生成二氧化碳2.2g.求:
(1)样品中氢氧化钠的质量;
(2)和氢氧化钠反应的盐酸的质量;
(3)在图中画出以纵坐标表示二氧化碳质量,横坐标表示盐酸的质量的关系图.

(已知Na2CO3+2HCl═2NaCl+H2O+CO2↑)
已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
[查阅资料]
铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2易溶于水);Fe、Cu不与氢氧化钠溶液反应.
[猜想]
猜想1:该合金粉末中除铝外,还含有铁、铜.
猜想2:该合金粉末中除铝外,还含有________(填名称).
猜想3:该合金粉末中除铝外,还含有铁.
[实验探究]
下列实验仅供选择的试剂:10% 盐酸、30% NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的________,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有________. |
| ②取步骤①所得滤渣,加过量的________,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有________. |
猜想1成立.
[实验反思]
一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.
[拓展延伸]
铜和稀硫酸在通常情况下不反应.但在特定条件下(如电解),铜和稀硫酸可以发生置换反应,并生成氢气.请写出此反应的化学方程式________.
某学习小组在探究CO2与NaOH溶液反应的实验中,先用铝制易拉罐收集满一罐CO2气体,然后迅速向其中加入-定量的30%NaOH浓溶液,立即将易拉罐口封闭(不漏气),轻轻摇动易拉罐,发现易拉罐很快变瘪,但过一段时间后,易拉罐又重新鼓起来(反应过程中温度的变化忽略不计).易拉罐开始时变瘪的原因是________(用化学方程式表示),易拉罐重新鼓起的原因是易拉罐中又生成了气体________.
某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由:______.
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应.
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了.该小组对这种意外现象的原因作了如下猜想:①可能是酚酞溶液与空气中的氧气反应,使红色消失;②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液.实验中“加热”和“滴入植物油”目的是______.实验结果表明酚酞溶液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:结论1:说明Na2CO3溶液呈______性;结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的NaOH溶液浓度过大:①实验方法______,②观察到的现象______.
方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.
该组同学将不同浓度的盐酸和NaOH溶液各10mL混合,用温
度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如表).
(1)表中x=______.
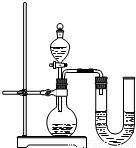
(2)某同学在没使用温度计的情况下,通过右图所示装置完成了实验.则该同学根据______判断NaOH溶液与稀盐酸发生了中和反应.
(3)关于实验中的细节和意外情况:①实验中,稀盐酸必须用胶头滴管逐滴滴加,这样做的目的是______.②实验过程中,要用玻璃棒不断搅拌,这样做的目的是______.③在实验过程中意外发现有气泡出现,你认为原因是______.④发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;你认为:②可能是______; ③可能是______.
(4)为了进一步研究实验中出现的问题,取了13.3g氢氧化钠固体样品加适量的水配成溶液,向其中加入200g10%的稀盐酸,使其充分反应,生成二氧化碳2.2g.求:
(1)样品中氢氧化钠的质量;______
(2)和氢氧化钠反应的盐酸的质量;______
(3)在图中画出以纵坐标表示二氧化碳质量,横坐标表示盐酸的质量的关系图.
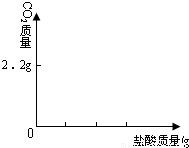
(已知Na2CO3+2HCl═2NaCl+H2O+CO2↑)
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由:______.
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应.
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了.该小组对这种意外现象的原因作了如下猜想:①可能是酚酞溶液与空气中的氧气反应,使红色消失;②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液.实验中“加热”和“滴入植物油”目的是______.实验结果表明酚酞溶液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:结论1:说明Na2CO3溶液呈______性;结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的NaOH溶液浓度过大:①实验方法______,②观察到的现象______.
方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.
该组同学将不同浓度的盐酸和NaOH溶液各10mL混合,用温
度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
(1)表中x=______.
(2)某同学在没使用温度计的情况下,通过右图所示装置完成了实验.则该同学根据______判断NaOH溶液与稀盐酸发生了中和反应.
(3)关于实验中的细节和意外情况:①实验中,稀盐酸必须用胶头滴管逐滴滴加,这样做的目的是______.②实验过程中,要用玻璃棒不断搅拌,这样做的目的是______.③在实验过程中意外发现有气泡出现,你认为原因是______.④发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;你认为:②可能是______; ③可能是______.
(4)为了进一步研究实验中出现的问题,取了13.3g氢氧化钠固体样品加适量的水配成溶液,向其中加入200g10%的稀盐酸,使其充分反应,生成二氧化碳2.2g.求:
(1)样品中氢氧化钠的质量;______
(2)和氢氧化钠反应的盐酸的质量;______
(3)在图中画出以纵坐标表示二氧化碳质量,横坐标表示盐酸的质量的关系图.

(已知Na2CO3+2HCl═2NaCl+H2O+CO2↑)