题目内容
某纯碱样品中含有少量的氯化钠杂质。现称取6g该纯碱样品放在烧杯中并滴加稀盐酸。当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如下图所示。试回答:
(1)A点产生气体的质量m = 。
(2)B点时,烧杯内溶液中的溶质是 (写出化学式)。
(3)A点时溶液中溶质的质量分数(写出计算过程,结果精确到0.1%)。
(1)2.2g (2)NaCl HCl (3)16.3%
解析试题分析:⑴ A点产生气体的质量m = 36.5g+6g-40.3g=2.2g ⑵盐酸添加到A点时碳酸钠恰好反应完全,溶液中溶质为氯化钠,再往其中添加盐酸则溶质为NaCl HCl。
⑶ 解:设原样品中含碳酸钠质量为x,反应生成氯化钠质量为y
Na2CO3 + 2HCl = 2NaCl+ H2O + CO2↑
106 117 44
x y 2.2g
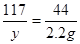
x = 5.3g y = 5.85g
6g-5.3g+5.85g = 6.55g 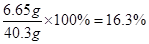
答: A点时溶液中溶质的质量分数为16.3%
考点:化学方程式的计算
点评:关于化学方程式的计算属于中考重点要求掌握的题型,每年必考,且以压轴题的形式出现,通常是数形结合,利用表格或者坐标曲线和题干相结合,一般只有最后一问较为困难,注意仔细审题。

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
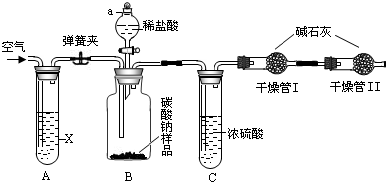
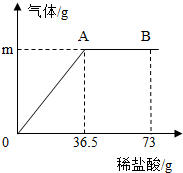 某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答: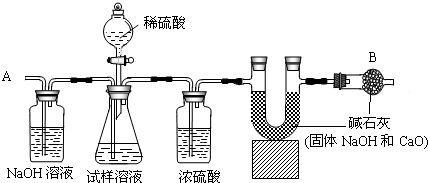
 如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:
如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算: (2013?贵港一模)某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
(2013?贵港一模)某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答: