题目内容
【题目】科学家尝试通过多种途径减少CO2的排放,或将CO2转化为有用的物质。其中一种途径是利用NaOH溶液来“捕捉”CO2,并将CO2储存或利用,反应流程如图所示。
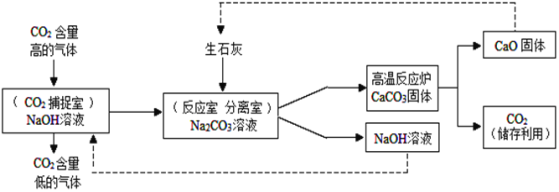
⑴反应分离室中分离物质的操作是__________。
⑵上述反应流程中,可循环利用的物质是__________。
⑶该过程至少发生了_______个化学反应,该流程中涉及到的基本反应类型有_______种。
⑷若反应分离室中有溶质质量分数为10.6%的Na2CO3溶液100kg,求完全反应后,理论上可生成CaCO3的质量(要求根据化学方程式计算)。______
【答案】过滤 NaOH和CaO 四 三 10kg
【解析】
⑴通过过滤可将难溶解的固体物质与液体分离。
⑵由反应流程示意图可知,上述反应流程中,NaOH和CaO既是反应物,又是生成物,所以NaOH和CaO是可循环利用的物质。
⑶该过程涉及到的反应有:2NaOH+CO2===Na2CO3 +H2O、CaO+H2O==Ca(OH)2、Na2CO3+Ca(OH)2==CaCO3↓+2NaOH、CaCO3![]() CaO+CO2↑四个化学反应,该流程中涉及到的基本反应类型有化合反应、复分解反应、分解反应三个。
CaO+CO2↑四个化学反应,该流程中涉及到的基本反应类型有化合反应、复分解反应、分解反应三个。
⑷100kg10.6%的Na2CO3溶液中所含碳酸钠的质量为:100kg×10.6%=10.6kg,设理论上可生成CaCO3的质量为x。
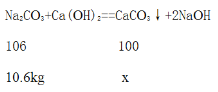
![]() =
=![]() ,解得x=10kg
,解得x=10kg

练习册系列答案
相关题目