题目内容
【题目】杂卤石(K2SO4MgSO42CaSO42H2O)属于“呆矿”,为能充分利用钾资源,用饱和的Ca(OH)2溶液浸杂卤石制备硫酸钾,工艺流程如下: 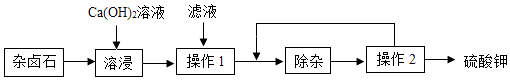
已知:
物质 | CaSO4 | K2SO4 | Mg(OH)2 |
溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(1)操作1的名称为 , 所需的玻璃仪器有玻璃棒、烧杯、 , 玻璃棒的作用是 .
(2)滤渣的主要成分有和 .
(3)“除杂”环节中,先加入溶液(填字母,下同),经搅拌等操作后,过滤,再加入 溶液调滤液pH至中性.
a.K2CO3 b.Na2CO3 c.稀硫酸 d.稀盐酸
(4)操作2的步骤是蒸发浓缩、、过滤、洗涤.
(5)洗涤硫酸钾最好选用 . a.30℃的水 b.饱和的硫酸钠溶液 c.饱和的硫酸钾溶液.
【答案】
(1)过滤;漏斗;引流
(2)Mg(OH)2;CaSO4
(3)a;c
(4)降温结晶
(5)c
【解析】解:(1)操作1的名称为过滤,所需的玻璃仪器有玻璃棒、烧杯、漏斗,玻璃棒的作用是引流. 故填:过滤;漏斗;引流.(2)滤渣的主要成分有氢氧化钙和硫酸镁反应生成的Mg(OH)2和溶解度较小的硫酸钙.
故填:Mg(OH)2;CaSO4 . (3)碳酸钾能和硫酸钙反应生成碳酸钙沉淀和硫酸钾,能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾,稀硫酸能和碳酸钾反应生成硫酸钾、水和二氧化碳,因此“除杂”环节中,先加入碳酸钾溶液,经搅拌等操作后,过滤,再加入稀硫酸.
故填:a;c.(4)操作2的步骤是蒸发浓缩、降温结晶、过滤、洗涤.
故填:降温结晶.(5)硫酸钾易溶于水,能够溶于饱和的硫酸钠溶液,不能溶于饱和的硫酸钾溶液,因此洗涤硫酸钾最好选用饱和的硫酸钾溶液.
故填:c.
(1)操作1的名称为过滤,通过过滤能够把固体和液体分离,所需的玻璃仪器有玻璃棒、烧杯、漏斗,玻璃棒的作用是引流;(2)根据物质的溶解度可以判断滤渣的成分;(3)碳酸钾能和硫酸钙反应生成碳酸钙沉淀和硫酸钾,能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾,稀硫酸能和碳酸钾反应生成硫酸钾、水和二氧化碳;(4)操作2的步骤是蒸发浓缩、降温结晶、过滤、洗涤;(5)硫酸钾易溶于水,能够溶于饱和的硫酸钠溶液,不能溶于饱和的硫酸钾溶液.

