题目内容
实验室欲配制50g5%的氧化钠溶液,现巳有仪器:①托盘天平、②药匙、③量筒(10mL、50mL,100mL),请根据要求填空.
(1)完成本实验,还需要的玻璃仪器有 .
(2)具体的操作步骤可简单概括为 .
(3)本实验量取蒸馏水时应选用 mL量筒.
(4)量筒读数时如果俯视,其他操作无误,则配制的溶液溶质质量分数将 (填“大于”、“小于”或“等于”)5%.
(5)如果所用的氯化钠中含有少很不溶性的杂质,则所配溶液溶质质量分数将会 (填“偏大”或“偏小”).
(1)完成本实验,还需要的玻璃仪器有
(2)具体的操作步骤可简单概括为
(3)本实验量取蒸馏水时应选用
(4)量筒读数时如果俯视,其他操作无误,则配制的溶液溶质质量分数将
(5)如果所用的氯化钠中含有少很不溶性的杂质,则所配溶液溶质质量分数将会
分析:根据溶液配制知识进分析,配制时使用的玻璃仪器主要是烧杯、量筒、玻璃棒;具体步骤可概括为:计算、称量、溶解;50g5%的氢氧化钠溶液含溶质的质量是50g×5%=2.5g,含水的质量是50g-2.5g=47.5g,即47.5mL;使用量筒读数时俯视导致量取得水少,溶质质量分数变大;所用的氯化钠中含有少很不溶性的杂质,会使溶质质量减少,溶质质量分数偏小.
解答:解:(1)配制时使用的玻璃仪器主要是烧杯、量筒、玻璃棒;故填:烧杯、玻璃棒;
(2)具体步骤可概括为:计算、称量、溶解;故填:计算、称量、溶解;
(3)50g5%的氢氧化钠溶液含溶质的质量是50g×5%=2.5g,含水的质量是50g-2.5g=47.5g,即47.5mL,所以量取蒸馏水时应选用50mL量筒;故填:50;
(5)使用量筒读数时俯视导致量取得水少,溶质质量分数变大;故填:大于;
(6)所用的氯化钠中含有少很不溶性的杂质,会使溶质质量减少,溶质质量分数偏小.故填:偏小.
(2)具体步骤可概括为:计算、称量、溶解;故填:计算、称量、溶解;
(3)50g5%的氢氧化钠溶液含溶质的质量是50g×5%=2.5g,含水的质量是50g-2.5g=47.5g,即47.5mL,所以量取蒸馏水时应选用50mL量筒;故填:50;
(5)使用量筒读数时俯视导致量取得水少,溶质质量分数变大;故填:大于;
(6)所用的氯化钠中含有少很不溶性的杂质,会使溶质质量减少,溶质质量分数偏小.故填:偏小.
点评:本题考查了溶液配制的有关内容,解答时可以依据相关知识进行解答,比较基础.

练习册系列答案
相关题目
 实验室欲配制50g5%的NaCl溶液,试回答下列问题.
实验室欲配制50g5%的NaCl溶液,试回答下列问题.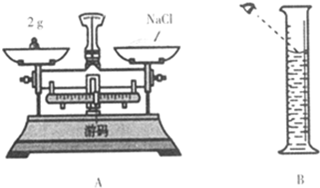 实验室欲配制50g5%的NaCl溶液,试回答下列问题.
实验室欲配制50g5%的NaCl溶液,试回答下列问题.