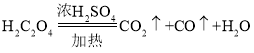题目内容
【题目】某种天然碱样品的化学式可以用xNaHCO3·yNa2CO3·zH2O表示(式中x、y、z是 最简整数比)。取50g某一浓度的盐酸与3.32g样品充分反应,能生成1.32gCO2气体。
(1)若改用1.66g样品与50g这种盐酸反应,能产生 gCO2。
(2)另取3.32g样品在300℃下加热至完全分解(已知:![]() , Na2CO3在300℃时不会分解),能产生0.22gCO2和0.45gH2O,试确定该样品的化学式: 。
, Na2CO3在300℃时不会分解),能产生0.22gCO2和0.45gH2O,试确定该样品的化学式: 。
(3)写出这种天然碱与盐酸完全反应的化学方程式。若6.64g天然碱样品与50g该盐酸能恰好完全反应放出,求该盐酸的溶质质量分数。
【答案】(1)0.66 (2)NaHCO3·2Na2CO3·2H2O (3)![]() 7.3%
7.3%
【解析】
天然碱与盐酸完全反应生成氯化钠、二氧化碳和水。
(1)50g某一浓度的盐酸与3.32g样品充分反应,能生成1.32gCO2气体,故改用1.66g样品与50g这种盐酸反应,能产生CO2的质量为![]() 。
。
(2)设样品中碳酸氢钠的质量为a,生成水的质量为b
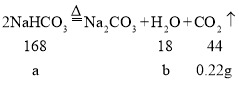
![]()
![]()
![]()
![]()
则样品中水的质量为![]() ,样品中碳酸钠的质量为
,样品中碳酸钠的质量为![]() ,xNaHCO3·yNa2CO3·zH2O中
,xNaHCO3·yNa2CO3·zH2O中![]() ,
,![]() ,故该样品的化学式为NaHCO3·2Na2CO3·2H2O。
,故该样品的化学式为NaHCO3·2Na2CO3·2H2O。
(3)这种天然碱与盐酸完全反应生成氯化钠、二氧化碳和水,故反应的化学方程式为![]() 。
。
设与6.64g天然碱样品恰好完全反应的氯化氢的质量为c
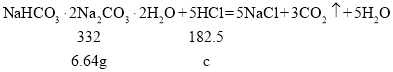
![]()
![]()
故该盐酸的溶质质量分数为![]() 。
。

练习册系列答案
相关题目