题目内容
【题目】某研究性学习小组为了测定某纯碱(假定杂质只有氯化钠)中Na2CO3的质量分数,称取10g纯碱固体,将其加入50g稀硫酸中,恰好完全反应,使气体全部放出,得到硫酸钠溶液56.7g.请你计算:
(1)反应中产生的CO2的质量是_____g。
(2)此纯碱样品中Na2CO3的质量分数___(写出必要的计算过程)。
【答案】3.3 79.5%
【解析】
(1)根据质量守恒定律,反应生成的二氧化碳的质量是:10g+50g-56.7g=3.3g;
(2)设纯碱中Na2CO3的质量为x

解得:x=7.95g
纯碱中Na2CO3的质量分数:![]() ×100%=79.5%;
×100%=79.5%;
答:(1)产生CO2的质量3.3g;(2)纯碱中Na2CO3的质量分数为79.5%。

练习册系列答案
相关题目
【题目】实验室有一部分被氧化成氧化镁的镁粉样品、未知浓度盐酸和40%的氢氧化钠溶液。兴趣小组同学为分析样品中金属镁的质量百分含量和计算盐酸的质量分株,进行如下探究:
(1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。实验数据如下表所示:
实验序号 | 所取样品质量(g) | 所加盐酸质量(g) | 生成氢气质量(g) |
Ⅰ | 16.0 | 60.0 | 0.5 |
Ⅱ | 16.0 | 130.0 | 1.0 |
Ⅲ | 16.0 | 150.0 | 1.0 |
镁粉样品中金属镁的质量百分含量为_________________。
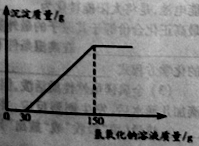
(2)向实验Ⅲ后的溶液中加入40%的氢氧化钠溶液,生成沉淀的质量随加入氢氧化钠溶液质量的变化关系如图所示。计算盐酸的质量分数。(写出计算过程)