题目内容
【题目】写出下列反应的化学方程式,并回答相关问题:
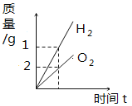
(1)在尘埃作用下二氧化硫与氧气反应_____________,各反应物和生成物化学计量数之和为________
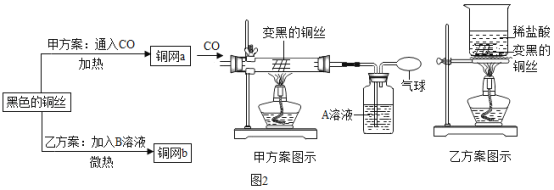
(2)湿法炼铜___________________,溶液颜色变化为________
(3)甲烷燃烧_____________,该反应_______(填吸热或放热)
(4)加热硝酸铵和氢氧化钠溶液的混合物_____________,生成的气体可用_________试纸检验
(5)用石灰乳吸收二氧化硫_________________,生成盐的名称为________
【答案】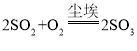 5
5 ![]() 蓝色溶液变成浅绿色
蓝色溶液变成浅绿色 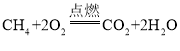 放热
放热 ![]() 湿润的红色石蕊试纸
湿润的红色石蕊试纸 ![]() 亚硫酸钙
亚硫酸钙
【解析】
(1)在尘埃作用下二氧化硫与氧气反应生成三氧化硫,该反应的化学方程式为: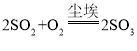 ;各反应物和生成物化学计量数之和为2+1+2=5;
;各反应物和生成物化学计量数之和为2+1+2=5;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:![]() ,溶液颜色的变化为:蓝色溶液变成浅绿色;
,溶液颜色的变化为:蓝色溶液变成浅绿色;
(3)甲烷燃烧生成了二氧化碳和水,反应的方程式是: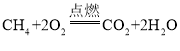 ;该反应放出热量;
;该反应放出热量;
(4)硝酸铵中滴加氢氧化钠溶液生成硝酸钠、水和氨气,反应的化学方程式为:![]() ,氨气属于碱性气体,故可用湿润的红色石蕊试纸检验;
,氨气属于碱性气体,故可用湿润的红色石蕊试纸检验;
(5)二氧化硫和氢氧化钙反应生成亚硫酸钙和水,反应的化学方程式![]() ;亚硫酸钙属于盐。
;亚硫酸钙属于盐。

【题目】同学们在学习碱的化学性质时,进行了如图所示的实验。
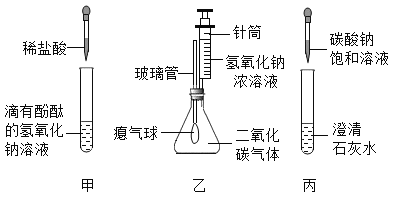
(1)上述甲、乙和丙各自独立反应后,溶质组成的种类可能最多的是_____________(选填甲、乙或丙)。
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是_____________。
(3)丙实验中观察到试管内有白色沉淀产生。
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问。
[提出问题]废液中含有哪些物质?
[交流讨论]①一定含有的物质:碳酸钙、指示剂、水和_____________(写物质名称)。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
[猜想]甲同学认为:只有氢氧化钠;
乙同学认为:只有氢氧化钙;
丙同学认为:是氢氧化钠和碳酸钠。
你认为还可能是_____________。(写一种合理猜想)
[实验设计]丁同学想用硝酸钙溶液来验证甲、乙和丙同学的猜想。查阅资料获悉硝酸钙溶液呈中性,并设计如下实验。请你将丁同学的实验设计补充完整。
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量硝酸钙溶液,静置 | ①无明显现象 | _____的猜想正确 |
②____________ | 丙同学的猜想正确 | |
③____________ | ______的猜想正确 |
[反思拓展]在分析化学反应后所得物质的成分时,需要考虑____________。