题目内容
【题目】根据图 1 装置,回答下列有关问题:
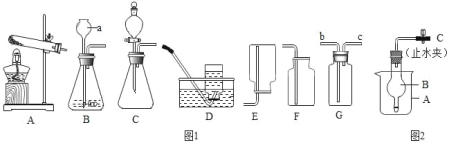
(1)装置图中仪器a的名称为 ________。
(2)写出以纯净物为原料用装置A制O2的化学方程式:________。
(3)氨气密度比空气小,极易溶于水,若用 G 装置采用排空气法收集NH3,氨气应从 ________口进(选“b”或“c”),若检验 NH3 是否集满,需将湿润的________色石蕊试纸放在 ____________管口。
(4)医用H2O2 在常温下难分解,但在双氧水溶液中加入铁锈,就会迅速分解,且反应结束后过滤出的铁锈可重复使用。试写出该反应的化学方程式:________。若需要控制该反应的速率,应选择的发生装置为 ________(填装置序号)。
某学生利用烧杯、球形干燥管和单孔橡皮塞等组成制取氢气的装置(如图 2),根据图2回答以下问题。
(5)实验室用锌粒和稀硫酸制取氢气的化学方程式为 _____。
(6)实验前,该装置 B 处应放的药品是 ____________。
(7)该装置的优点是____________(只需回答一点)。
(8)若使正在发生的反应停止,可以通过________来实现(写出操作过程)。
【答案】长颈漏斗 2 KMnO4![]() K2MnO4 + MnO2 + O2↑ c 红 b 2 H2O2
K2MnO4 + MnO2 + O2↑ c 红 b 2 H2O2 ![]() 2H2O + O2↑ C Zn + H2SO4 = ZnSO4 + H2↑ 锌粒 控制反应的发生与停止 将B提起来或关闭止水夹
2H2O + O2↑ C Zn + H2SO4 = ZnSO4 + H2↑ 锌粒 控制反应的发生与停止 将B提起来或关闭止水夹
【解析】
(1)仪器a是长颈漏斗;故填:长颈漏斗;
(2)实验室制氧气的药品有:高锰酸钾,氯酸钾和二氧化锰,双氧水和二氧化锰,其中反应试剂为纯净物的是高锰酸钾,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故填:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)氨气的密度比空气小,多功能瓶排空气法收集氨气要短进长出;若检验NH3是否集满,需将湿润的红色石蕊试纸放在b管口,如果湿润的红色石蕊试纸变蓝,说明氨气已经收集满。故填:c;红;b;
(4)过氧化氢在铁锈做催化剂的条件下生成水和氧气,要注意配平;装置C的分液漏斗可以通过控制液体的滴加速度从而控制反应的速率;故答案为:2H2O2![]() 2H2O+O2↑;C;
2H2O+O2↑;C;
(5)实验室制氢气的原理是锌粒和稀硫酸反应生成氢气和硫酸锌;故填:Zn+H2SO4=ZnSO4+H2↑;
(6)该装置B处应放的药品是锌粒,因为锌是固体;故填:锌粒;
(7)将球形干燥管放入烧杯中,烧杯中的液体药品与球形干燥管中的固体接触反应开始,可通过将球形干燥管提高来实现固液分离从而使反应停止。该装置的优点是能够控制反应的发生和停止;故填:控制反应的发生与停止;
(8)若使正在发生的反应停止,可以通过关闭止水夹,或将球形干燥管提起来,使固液分离等来实现。故填:B提起来或关闭止水夹。

【题目】
(1)如图为“**泡打粉”标签
| (2)如图为“胃酸完全抑制剂”标签 |
①碳酸氢钠俗称____________。 ②加入泡打粉制作的蛋糕更松软,其原理可用化学方程式表示为:3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3X↑,则X的化学式为____________。 | ①氢氧化镁和胃酸发生的反应为:Mg(OH)2+2HCl═MgCl2+2H2O,该反应的基本类型是____________反应。 ②碳酸钙与胃酸反应的化学方程式为____________。 |