题目内容
【题目】人类生活离不开金属。
(1)铁是生活中常用的金属。如图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热。

①发热剂需接触到空气才会发热,原因是铁要与_____、_____等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是__________________。
(2)应用金属活动性顺序能帮助我们进一步学习金属性质。
已知下列各组物质间均能发生置换反应。
AFe 和CuSO4 溶液 BMg和MnSO4 溶液 CMn和FeSO4 溶液
①写出Fe和CuSO4溶液反应的化学方程式__________________。
【答案】水 氧气 加速铁粉生锈,更快的放出热量 Fe+CuSO4=FeSO4+Cu
【解析】
(1)①铁生锈需要与潮湿的空气接触,实际上是和潮湿的空气中的氧气和水发生化学反应。故答案为:水、氧气;
②当有盐溶液存在时,铁生锈的速度加快,所以发热剂中加入一定的氯化钠,可以加速铁的锈蚀,从而更快的放出热量。故答案为:加速铁粉生锈,更快的放出热量;
(2)①铁的金属活动性顺序比铜强,可以置换出硫酸铜中的铜,发生置换反应。铁和硫酸铜反应生成硫酸亚铁和铜。故答案为:Fe+CuSO4=FeSO4+Cu。

【题目】碳酸钠、碳酸氢钠是生活中两种常见的重要的盐。
(1)碳酸钠(俗称纯碱、苏打)与碳酸氢钠(俗称_____),均为________色固体,水溶液均呈_______性,向它们的水溶液中分别滴入无色酚酞试液,酚酞试液均变红色。
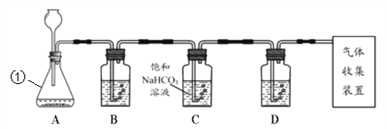
(2)碳酸钠、碳酸氢钠均可与稀盐酸反应,其中碳酸钠与稀盐酸反应的化学方程式为_____。但是,碳酸钠、碳酸氢钠与稀盐酸反应产生二氧化碳的速率是否相同?校兴趣小组同学针对于此,展开探究:
(方案设计)
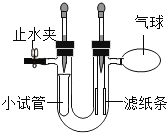
①甲设计的实验如图1所示,实验时,同时全部推出足量稀盐酸后,观察到图2所示现象。于是他得出______和稀盐酸反应产生二氧化碳较快的结论。
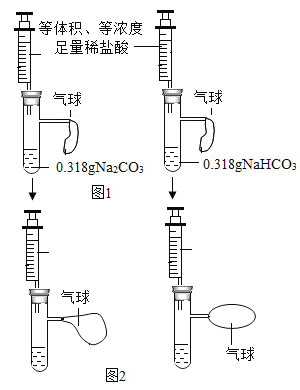
②乙同学通过计算可知:0.318 g碳酸氢钠约产生0.167 g二氧化碳,而0.318 g碳酸钠产生二氧化碳的质量为______g,等质量的碳酸钠与碳酸氢钠与足量的稀盐酸作用,碳酸氢钠产生二氧化碳的质量更多,显然甲同学的设计不妥,应取含碳元素质量相同的碳酸钠和碳酸氢钠进行实验。若碳酸钠的质量仍为0.318g,应称取碳酸氢钠的质量为_______g。
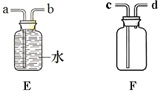
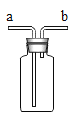
③小组同学在老师指导下设计了图3所示实验。连通管除消除稀盐酸滴入占有体积引起的误差,还有______的作用。
分别取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠稀溶液(各滴2滴酚酞溶液)以及相同体积、相同浓度的足量稀盐酸进行实验。实验时,广口瓶内压强随时间变化如图4所示,溶液颜色变化记录如表1。
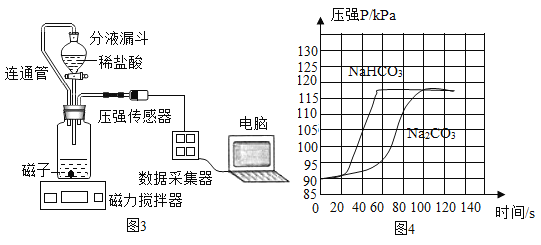
表1:
滴入酚酞溶液 | 滴入稀盐酸,溶液颜色变化 | |
碳酸钠溶液 | 红色 | 红色→浅红色→无色 |
碳酸氢钠溶液 | 浅红色 | 淺红色→无色 |
(实验结论)分析图4所示的实验数据可得到:相同条件下,碳酸氢钠与稀盐酸反应产生二氧化碳速率更快,你判断的理由是_______。
(实验反思)小组同学分析表1实验现象和图4数据,得出碳酸钠能与稀盐酸反应产生二氧化碳,反应是分步进行的。第一步发生的化学反应方程式是:_______,第二步发生的反应是:NaHCO3+HCl=NaCl+H2O+CO2↑。