题目内容
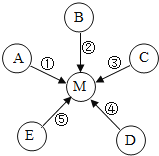
【题目】金属(Ti)硬度大、熔点高、耐腐蚀,被誉为“未来的金属”钛酸亚铁(FeTiO3)过一系列反应制备钛和纳米Ti02,主要生成过程如下:

(1)钛酸亚铁中钛元素的化合价为______价;
(2)反应②生成TiCl4和一种有毒的气体,该气体是一种氧化物,其化学式为________
(3)反应③属于置换反应,写出该反应的化学方程式:_____________________
(4)生产过程中的反应可能是分解反应的是__________(填序号),
(5)近年来,利用电解熔融TiO2的方法来制备金属钛获得成功,从能量的角度分析,工业
上利用该方法制备钛的主要缺点是___________
【答案】(1)+4 (2)CO (3)TiCl4+2Mg 高温 Ti+2MgCl2 (3)⑤ (4)消耗大量的电能,浪费能源
【解析】
试题分析:(1)根据化合物中,化合价的代数和为零,可设钛的化合价为x,则(+2)+x+(-2)×3=0 x=+4
根据质量守恒定律可知,反应前后元素的种类不变,因此有毒的气体为CO
据题意可知生成物为单质和化合物,可写出化学方程方程为:TiCl4+2Mg 高温 Ti+2MgCl2 。
因为只有反应⑤ 的反应物是一种,所以只有此反应为分解反应。
(5)利用电解熔融TiO2的方法来制备金属钛获得成功,从能量的角度分析要消耗大量的电能,浪费能源。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目