题目内容
【题目】(6分)“对比实验”是化学学习中行之有效的思维方法。某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题。
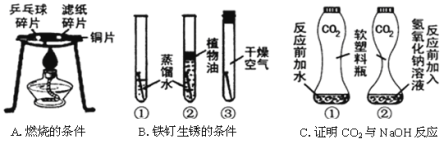
(1)通过实验A,可以说明燃烧的条件之一是 ,实验中使用铜片,是利用了铜的 性(填写物理性质)。
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与水
和 直接接触。通常用酸洗的方法除去铁锈,铁制品除锈时 (填写“能”或“不能”)长时间浸在酸溶液中。
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 。
【答案】(1)温度达到可燃物的着火点 导热性 (2)氧气 不能 (3)2NaOH+CO2=Na2CO3+H2O
【解析】
试题分析:(1)通过实验A看到的现象:铜片上的乒乓球碎片燃烧,而滤纸碎片不燃烧,可以说明燃烧的条件之一是温度达到可燃物的着火点;实验中使用铜片,是利用了铜的导热性
(2)对于实验B,试管①和②比较,试管②没有空气,铁不生锈,试管①和③比较,试管③没有水,铁不生锈,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与水和氧气直接接触;用酸洗的方法除去铁锈,铁制品除锈时不能长时间浸在酸溶液中,因为酸会与铁继续反应:Fe + 2HCl = FeCl2 + H2↑
(3)CO2与NaOH溶液反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目