题目内容
某研究性学习小组探究下列化学反应的特征:
(I)KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
(Ⅱ)FeS+HNO3→Fe(NO3)3+Fe2(SO4)3+NO2↑+N2O4↑+NO↑+H2O
(Ⅲ)CuSO4→CuO+SO3↑+SO2↑+O2↑
(Ⅳ)CO2+KOH→KHCO3+K2CO3+H2O
(1)大多数化学反应中物质的化学计量数之比是固定的,但上述化学反应的化学计量数之比是不确定的,即物质的化学计量数有多组.根据上述实例,请用一句话归纳化学计量数有多组的化学反应的特点:________.
(2)反应(Ⅱ)中还原产物是 ________,若其物质的量之比确定,该反应的化学计量数也随之确定.
(3)有人认为反应(Ⅲ)是两个反应式加合的结果,请分析它是哪两个化学反应加合而成的:________、________.在反应(Ⅲ)中,根据电子转移守恒,物质 ________和 ________的物质的量之比是固定的.
(4)若将16gCuSO4固体粉末按反应(Ⅲ)完全分解,最终气体产物的物质的量的取值范围是:________.
(5)若反应(Ⅳ)中KHCO3、K2CO3的化学计量数分别为a、b,则用a、b表示该反应的化学计量数的化学方程式是 ________.
解:(1)由(3)题中暗示可知,化学计量数有多组的化学反应的特点为一个反应可视为2个或多个反应的加合.
故答案为:一个反应可视为2个或多个反应的加合.
(2)根据化合价降低的是氧化剂,我们知道HNO3是氧化剂,氧化剂在化学反应中被还原,生产的物质是还原产物,故答案为:NO2、N2O4、NO
(3)化学反应在加合时,反应物和反应物加合,生成物和生成物加合,故答案为:CuSO4?CuO+SO3↑,2SO3 2SO2+O2,SO2和O2
2SO2+O2,SO2和O2
(4)依据硫酸铜的分子量是160,我们可以计算16gCuSO4固体粉末的物质的量是0.1moL,
根据配平以后的化学反应4CuSO4=4CuO+2SO3↑+2SO2↑+O2↑可以计算,故答案为:(0.1,0.15)
(5)根据反应前后原子的种类和数目不变,可以将CO2+KOH→KHCO3+K2CO3+H2O配平为
(a+b)CO2+(a+2b)KOH=aKHCO3+bK2CO3+(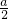 +b)H2O.故答案为:(a+b)CO2+(a+2b)KOH=aKHCO3+bK2CO3+(
+b)H2O.故答案为:(a+b)CO2+(a+2b)KOH=aKHCO3+bK2CO3+(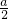 +b)H2O
+b)H2O
分析:此题在学生已有知识的基础上,让学生进一步探究化学反应的有关问题.根据质量守恒定律进行化学方程式的有关配平和计算,反应前后原子的种类和数目不变.
点评:本题重点围绕化学反应前后原子的种类和数目不变考查学生们的配平能力,是一道不错的题目.
故答案为:一个反应可视为2个或多个反应的加合.
(2)根据化合价降低的是氧化剂,我们知道HNO3是氧化剂,氧化剂在化学反应中被还原,生产的物质是还原产物,故答案为:NO2、N2O4、NO
(3)化学反应在加合时,反应物和反应物加合,生成物和生成物加合,故答案为:CuSO4?CuO+SO3↑,2SO3
 2SO2+O2,SO2和O2
2SO2+O2,SO2和O2(4)依据硫酸铜的分子量是160,我们可以计算16gCuSO4固体粉末的物质的量是0.1moL,
根据配平以后的化学反应4CuSO4=4CuO+2SO3↑+2SO2↑+O2↑可以计算,故答案为:(0.1,0.15)
(5)根据反应前后原子的种类和数目不变,可以将CO2+KOH→KHCO3+K2CO3+H2O配平为
(a+b)CO2+(a+2b)KOH=aKHCO3+bK2CO3+(
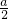 +b)H2O.故答案为:(a+b)CO2+(a+2b)KOH=aKHCO3+bK2CO3+(
+b)H2O.故答案为:(a+b)CO2+(a+2b)KOH=aKHCO3+bK2CO3+(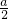 +b)H2O
+b)H2O分析:此题在学生已有知识的基础上,让学生进一步探究化学反应的有关问题.根据质量守恒定律进行化学方程式的有关配平和计算,反应前后原子的种类和数目不变.
点评:本题重点围绕化学反应前后原子的种类和数目不变考查学生们的配平能力,是一道不错的题目.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.
某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物. 34、某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.
34、某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.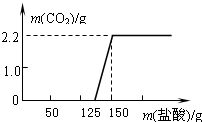 某研究性学习小组探究实验室中久置的NaOH的变质程度,先称取一定质量的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.
某研究性学习小组探究实验室中久置的NaOH的变质程度,先称取一定质量的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.