题目内容
【题目】正确的实验操作是实验成功的保证,下列实验操作正确的是( )
A. CO2验满
CO2验满
B. 收集O2
收集O2
C.![]() 滴加液体
滴加液体
D.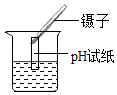 测溶液pH
测溶液pH
【答案】B
【解析】解:A.验满二氧化碳时燃烧的木条不能伸入瓶内,故A错误;
B.由于氧气不易溶于水且密度比水的小,故应用图示装置收集氧气时应从短进长出,故B正确;
C.滴管不能伸入试管内,故C错误;
D.测定溶液的pH时,不能把试纸直接浸入溶液内,会把溶液污染,故D错误.
故选B.
【考点精析】解答此题的关键在于理解液体药品取用的方法的相关知识,掌握液体药品的取用:①液体试剂的倾注法②液体试剂的滴加法,以及对氧气的收集方法的理解,了解收集装置:根据物质的密度、溶解性;排水法收集时,待气泡均匀连续冒出时再收集(刚开始排出的是试管中的空气;)用排空气法收集气体时,导管伸到集气瓶底部.

【题目】反思、归纳与提升是化学学习的重要方法.
(1)对于复分解反应及其规律,通过反思与探索,同学们有了新的认识. 【探索发现】①氢氧化钠溶液与盐酸反应的微观示意图如图1;
【分析归纳】反应的化学方程式
反应的实质:H++OH﹣═H2O,反应能进行的原因是溶液中的H+和OH﹣的数目减少,即自由移动的离子数目减少.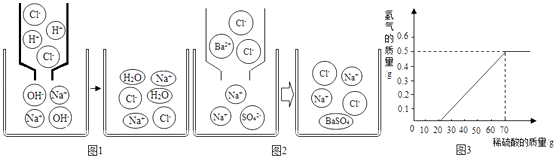
②硫酸钠溶液跟氯化钡溶液反映的微观示意图如图2:
【分析归纳】反应的化学方程式为:Na2SO4+BaCl2═2NaCl+BaSO4↓.反应能进行的原因是溶液中的数目减少,即自由移动的离子数目减少.(提示:生成硫酸钡白色沉淀)
【总结规律】上述复分解反应能发生的本质原因是 .
(2)某同学利用以下几组物质探究硫酸的性质
组合序号 | ① | ② | ③ | ④ | ⑤ |
组合物质 | H2SO4 | H2SO4 | H2SO4 | H2SO4 | H2SO4 |
【记录和解释】待几组物质恰好完全反应后,往溶液中滴加紫色的石蕊溶液,其中组合与另外四组现象不同,请从反应发生的本质角度解释产生不同现象的原因 .
(3)某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应,测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质). ①当稀硫酸的质量为70g,产生的氢气的质量为g.
②用化学方程式说明当稀硫酸的质量为10g时,为什么不产生氢气 .
③计算镁条中镁元素的质量分数(写出计算过程).