题目内容
小明做红磷燃烧实验,需要氧气0.2g.(氧气密度为1.43g/L)(1)实验时,为了保证所需的氧气量,他大致需要空气______mL.(结果保留整数)
(2)为了得到浓度较大的氧气,小明思考了一下,改用下面的方法来收集氧气:
第一步:取250毫升的集气瓶,预先使瓶内留有占其容积的20%的水(余下为空气),用玻片盖住瓶口,并倒立于水槽中.
第二步:向瓶中小心通入氧气,待瓶内水排完后,用玻片盖住瓶口,取出正放好.
请帮小明计算一下,瓶内氧气的量能否满足实验的需要?(写出计算过程及结果)
(3)若小明按一定比例将氯酸钾和二氧化锰混合加热制取氧气,请在坐标系中画出反应过程中二氧化锰的质量分数(%)随时间(t)而变化的图象.
【答案】分析:(1)根据氧气的质量和密度计算出氧气的体积,因氧气的体积占空气体积的21%,即可求得空气的体积;
(2)第一步:取250毫升的集气瓶,求得其80%体积的空气中氧气的体积;第二步:在250毫升的集气瓶里占其容积的20%的水全部排净变为氧气;根据这两步操作中氧气的总量再求得空气的体积,然后比较可得所需结果.
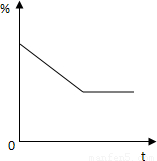
(3)因二氧化锰在此反应中作催化剂,其质量在反应前后始终不变,而将一定比例将氯酸钾和二氧化锰混合加热时,混合物的质量不断减少直至氯酸钾分解完毕,由题意可画出其变化图象.
解答:解:(1)需要氧气0.2g时,(氧气密度为1.43g/L)所需空气的体积:
0.2g÷1.43g/L÷21%=0.666L=666mL
(2)计算这两步操作中氧气的体积和能存在于空气的体积比较:250mL×(1-20%)×21%+250mL×2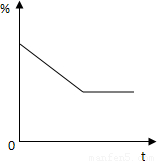 0%=92mL 92mL÷21%=438mL<666mL 不满足实验的需要.
0%=92mL 92mL÷21%=438mL<666mL 不满足实验的需要.
(3)有分析画出图象是:
故答案为:
(1)666mL;
(2)250mL×(1-20%)×21%+250mL×20%=92mL 92mL÷21%=438mL<666mL 不满足实验的需要;
(3)
点评:本题考查学生根据氧气占空气体积分数进行分析解题的能力.特别注意二氧化锰在反应中作催化剂,其质量在化学反应前后不变,根据反应事实绘画图象.
(2)第一步:取250毫升的集气瓶,求得其80%体积的空气中氧气的体积;第二步:在250毫升的集气瓶里占其容积的20%的水全部排净变为氧气;根据这两步操作中氧气的总量再求得空气的体积,然后比较可得所需结果.
(3)因二氧化锰在此反应中作催化剂,其质量在反应前后始终不变,而将一定比例将氯酸钾和二氧化锰混合加热时,混合物的质量不断减少直至氯酸钾分解完毕,由题意可画出其变化图象.
解答:解:(1)需要氧气0.2g时,(氧气密度为1.43g/L)所需空气的体积:
0.2g÷1.43g/L÷21%=0.666L=666mL
(2)计算这两步操作中氧气的体积和能存在于空气的体积比较:250mL×(1-20%)×21%+250mL×2
 0%=92mL 92mL÷21%=438mL<666mL 不满足实验的需要.
0%=92mL 92mL÷21%=438mL<666mL 不满足实验的需要.(3)有分析画出图象是:
故答案为:
(1)666mL;
(2)250mL×(1-20%)×21%+250mL×20%=92mL 92mL÷21%=438mL<666mL 不满足实验的需要;
(3)

点评:本题考查学生根据氧气占空气体积分数进行分析解题的能力.特别注意二氧化锰在反应中作催化剂,其质量在化学反应前后不变,根据反应事实绘画图象.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
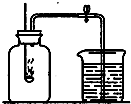 小明同学利用如图装置测定空气中氧气的含量,请你分析小明进行下列操作的理由:在带橡皮塞和导管的燃烧匙内装满红磷
小明同学利用如图装置测定空气中氧气的含量,请你分析小明进行下列操作的理由:在带橡皮塞和导管的燃烧匙内装满红磷 小明做红磷燃烧实验,需要氧气0.2g.(氧气密度为1.43g/L)
小明做红磷燃烧实验,需要氧气0.2g.(氧气密度为1.43g/L) 小明同学利用如图装置测定空气中氧气的含量,请你分析小明进行下列操作的理由:在带橡皮塞和导管的燃烧匙内装满红磷________,将胶管上的止水夹夹紧,把燃烧匙内的红磷放在酒精灯火焰上点燃,并迅速伸入集气瓶内________,塞紧橡皮塞,________.
小明同学利用如图装置测定空气中氧气的含量,请你分析小明进行下列操作的理由:在带橡皮塞和导管的燃烧匙内装满红磷________,将胶管上的止水夹夹紧,把燃烧匙内的红磷放在酒精灯火焰上点燃,并迅速伸入集气瓶内________,塞紧橡皮塞,________.