题目内容
【题目】某活动小组的同学利用氯酸钾和二氧化锰共热制取一定量的氧气。混合27.6g氯酸钾和2.0g二氧化锰,加热制取一定量的氧气后,停止反应,测得剩余固体中二氧化锰的质量分数为10%。请计算:
(1)剩余固体的质量_____________________________________。
(2)制得氧气的质量______________________________________。
(3)未分解的氯酸钾的质量______________________。
【答案】20g9.6 g解:设参加反应的氯酸钾的质量为x
2KClO3 ![]() 2KCl+3O2↑ ………………………………… 1分
2KCl+3O2↑ ………………………………… 1分
245 96
x 9.6g ………………………………… 1分
245/x=96/9.6g ………………………………… 1分
x=24.5g ………………………………… 1分
未分解的氯酸钾的质量为:27.6g—24.5g=3.1g …………………… 1分
答:未分解的氯酸钾的质量为3.1g。
【解析】(1)二氧化锰为催化剂,反应前后质量不变,且又知反应后二氧化锰的质量分数为10%,由此反应后固体的质量=2.0g÷10%=20g;(2)由质量守恒定律氯酸钾的质量+二氧化锰的质量=氯化钾的质量+二氧化锰的质量+氧气的质量,又反应后固体质量为20g,那么氧气的质量=27.6g+2.0g-20g=9.6g;(3)氯酸钾反应前质量为27.6g,那么根据方程式求出已经分解的氯酸钾的质量,剩余即为未分解的氯酸钾;

【题目】人类的生活和生产都离不开金属材料。
(一)铁材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是_________。
(2)下列说法不正确的是________________。(填字母序号)
A.铁丝在氧气中剧烈燃烧,火星四射,生成氧化铁;
B.回收废旧金属有利于节约金属资源;
C.在铁桶中加入硫酸铜溶液和石灰乳来配制农药波尔多液。
D.铁锅常用于炒饭炒菜,是利用了铁的导热性
铁制品锈蚀的过程,实际上是铁与空气中的_____________________等发生化学反应的过程。请写出一种防锈措施 __________________________________。
(二)请你参与探究几种常见金属饰品所含金属的相关活动,并回答下列问题。
现用一定量的AgNO3和Cu(NO3)2混合溶液,进行了如右图所示的实验,并对溶液A和固体B的成分进行了分析和研究。
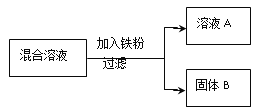
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】
①只有Fe(NO3)2 ②有Fe(NO3)2 、AgNO3
③有Fe(NO3)2 、Cu(NO3)2 ④有___________________________。
【交流讨论】不合理的猜想是_______________(填标号)。
【实验探究】根据下表中的实验步骤及现象,完成表中的实验结论
实验步骤 | 现象 | 实验结论 |
取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想____________, 固体B中的金属成分为____________(写化学式)。 |
【数据处理】称取10克固体B于烧杯中,向烧杯中加入100克稀硫酸,恰好完全反应后称得烧杯内混合物的总质量为109.8克。请计算
(1)所用稀硫酸的溶质质量分数为多少?(请写出计算过程)
______
(2)若配制上述浓度的稀硫酸100克,则需质量分数98%的浓硫酸______克。