题目内容
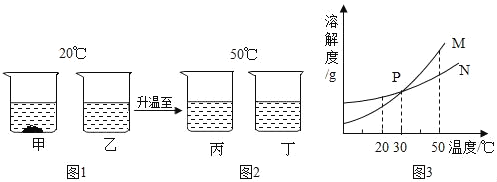
【题目】关于如图两种物质的溶解度曲线说法正确的是( )

A. 升高温度,可使甲的不饱和溶液变为饱和溶液
B. 50℃时甲的饱和溶液溶质的质量分数为40%
C. 要使乙从其浓溶液中析出,可冷却乙的热浓溶液
D. 20℃时,甲、乙两种物质的溶解度相等
【答案】D
【解析】
A、由于甲的溶解度随温度的升高而增大,因此升温会使甲的不饱和溶液变得更不饱和,选项错误;
B、在50℃时,甲的溶解度是40g,则该温度下,甲的饱和溶液中溶质的质量分数为:![]() ×100%≈28.6%,选项错误;
×100%≈28.6%,选项错误;
C、由于乙的溶解度随温度的降低而增大,因此若想使乙从它的浓溶液中析出,不能采取降温的方法,可以采用升温的方法,选项错误;
D、从溶解度曲线可以看出,20℃时,甲、乙两种物质的溶解度相等,选项正确,故选D。

【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
【题目】t1℃时,将甲、乙、丙三种固体各20克,分别加入盛有50克水的烧杯中,充分溶解后的情况如下表
物质 | 甲 | 乙 | 丙 |
未溶解的固体/g | 5.4 | 0 | 2 |
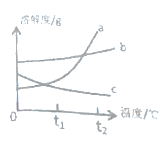
(1)一定是饱和溶液的是_______,t1℃时丙的溶解度为_______。
(2)图中表示固体甲的曲线是________。
(3)t1℃时,甲乙丙的溶解度大小关系为_______。
(4)t2℃时,取等质量的甲乙丙的饱和溶液,分别恒温蒸发等质量的水,析出溶质质量的大小关系为______(用甲乙丙表示)