题目内容
【题目】在一次探究实验中,某学习小组将a 克高锰酸钾充分加热至不再放出气体为止,若试管中剩余固体的质量随时间变化关系如图所示。请计算:
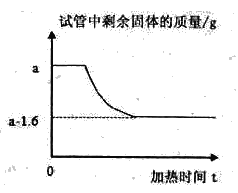
(1)根据质量守恒定律,反应生成氧气的质量为_______g。
(2)该小组加入的高锰酸钾的质量(即a克)是多少_______?(要求写出计算过程)
(3)反应后剩余固体中钾、锰两种元素的质量比为__________。
【答案】1.6 15.8g 39:55
【解析】
(1)根据质量守恒定律,固体减少的质量为反应生成氧气的质量,故反应生成氧气的质量为1.6g。
(2)设加入的高锰酸钾的质量为x,则

![]()
解得x=15.8g;
答:该小组加入的高锰酸钾的质量为15.8g。
(3)反应后剩余固体中钾、锰两种元素的质量的质量不变,仍然和高锰酸钾中钾、锰元素的质量相同,故其质量比为39:55。

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
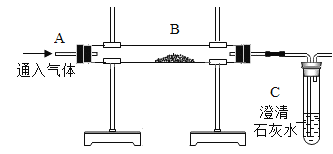
【题目】实验室常用的制取二氧化碳气体的研究如下:
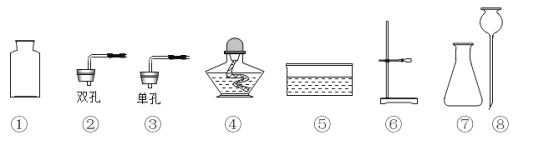
(1)仪器问题:制取二氧化碳的发生装置,除了用到⑦号仪器外,还需选择的仪器是________(填序号)。收集二氧化碳,用如图装置收集时,空气从_____(选填“x”或“y”)端排出。
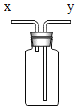
(2)装置改进:
仪器a的名称是_______;使用其优点为__________;改进装置的优点是_________________(写一条即可)。
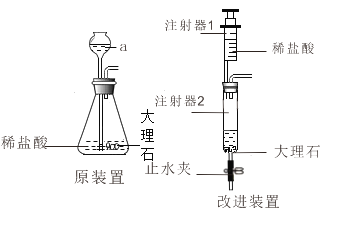
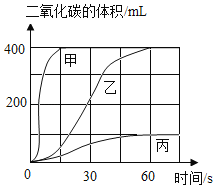
(3)选用药品:按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如图所示:
实验编号 | 药品 |
Ⅰ | 块状大理石、10%H2SO4溶液 |
Ⅱ | 块状大理石、7%HCl溶液 |
Ⅲ | 大理石粉末、7%HCl溶液 |
图中丙对应实验_____(选填“I”“Ⅱ”或“Ⅲ”)。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是________;不用甲对应的药品,理由是________。