题目内容
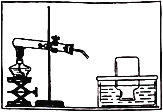
【题目】41中学化学小组的同学在学习有关酸的化学性质时进行了如图所示的实验:
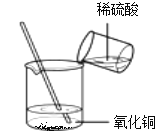
请你写出实验中所发生的化学方程式(1)____________________。
(提出问题)反应后溶液中的溶质是什么?
(猜想与假设)
文博同学的猜想:CuSO4
博文同学的猜想:CuSO4、CuO、H2SO4
你的猜想:(2)____________
请你评价博文同学的猜想(3)____________。
(实验探究)宇航同学取反应后的溶液加入足量的氢氧化钠溶液,观察到有蓝色沉淀生成,请写出一定发生反应的化学方程式(4)_____________,于是认为文博同学的猜想正确。通过大家的交流,一致认为宇航同学的实验及结论是错误的,请你说明理由(5)___________。
(反思与评价)探究化学反应所得溶液中溶质成分时,通过书写化学方程式能做出初步判断:(6)____一定存在,(7)____可能存在,然后设计实验进行探究,得出正确结论。
【答案】CuO+H2SO4==CuSO4+H2O CuSO4、H2SO4 不正确,CuO不溶于水,所以溶质中不能存在。 2NaOH+CuSO4===Cu(OH)2↓+Na2SO4 加入足量的氢氧化钠溶液产生蓝色沉淀,说明溶液中含有硫酸铜,但氢氧化钠与硫酸反应无明显现象,无法判断是否含有硫酸。 可溶性产物 可溶性反应物
【解析】
(1)氧化铜和硫酸反应生成硫酸铜和水,发生的化学方程式:CuO+H2SO4=CuSO4+H2O;
(2)若硫酸过量,反应后溶液中的溶质是CuSO4、H2SO4;
(3)因为氧化铜难溶于水,即使有剩余,反应后溶液中不会有氧化铜;
(4)氢氧化钠和硫酸铜生成氢氧化铜沉淀和硫酸钠,发生的化学方程式:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(5)氢氧化钠与硫酸反应生成硫酸钠和水,没有明显现象,所以:加入足量的氢氧化钠溶液产生蓝色沉淀,说明溶液中含有硫酸铜,但氢氧化钠与硫酸反应无明显现象,无法判断是否含有硫酸;
(6)(7)由“CuO+H2SO4=CuSO4+H2O;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;氢氧化钠与硫酸反应生成硫酸钠和水,没有明显现象”分析可知:可溶性的生成物能鉴别存在,而可溶性的反应物有时鉴别不出来。

 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案