题目内容
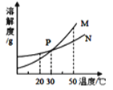
【题目】在 20℃时,将等质量的甲、乙两种固体分别加入盛有 100 g 水的烧杯中,充分搅拌后的现象如左图所示,甲、乙两物质的溶解度曲线如右图所示。则下列说法正确的是( )
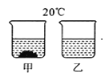
A. 烧杯甲中的溶液是N 溶液
B. 烧杯乙的溶液一定是不饱和溶液
C. 烧杯甲的溶液升温到 30℃时,烧杯底部还有部分物质不溶解
D. 若烧杯甲和烧杯乙的溶液都升温到 30℃时溶质的质量分数相等
【答案】D
【解析】
由图可知20℃时M的溶解度小于N,相同条件下溶解度小的溶解的少,所以甲烧杯中是M,A选项错误;烧杯乙中的溶液可能恰好饱和,B选项错误;M、N两物质在30℃时溶解度相同,所以甲烧杯升温到30℃,应该和乙烧杯的现象相同,固体全部溶解,C选项错误;甲乙烧杯升温到30℃,溶解度相同,溶质质量相同,故溶质的质量分数相同,D选项正确;故选择D项。

【题目】分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)氯化钠的溶解度曲线是 _________(填“甲”或“乙”)。
(2)20℃时,将40g NH4Cl加入100g的水中,充分搅拌后得到的是______溶液(填“饱和”或“不饱和”),将上述溶液升温到30℃,该溶液的溶质质量分数为_______(只列计算式,不需要计算结果)。
(3)如下图,t1℃时,将两种物质的饱和溶液各100g,分别恒温蒸发5g水,析出晶体最多的是______(填“甲”或“乙”)。

(4)计算配制50g质量分数为3%的NaCl溶液所需质量分数为6%的NaCl溶液的体积,需要用到的数据是_____________(填字母)。
A.3%的NaCl溶液的密度 B.水的密度 C.6%的NaCl溶液的密度
【题目】钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:___________________________;
(2)实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
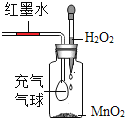
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4 ![]() CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
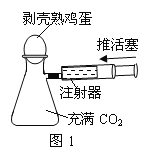
③常温下,Ca(OH)2微溶于水;于是他设计了下图的实验装置,结合装置回答下列问题:
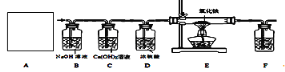
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的_________(填装置编号);
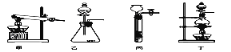
(2)图中装置C、D的作用分别是 ____________、_______________;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的_____________(填试剂名称),反应的化学方程式为 ______________________;
(4)该装置设计有一个明显缺陷,你认为是______________________________。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下:
![]()
根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;②_________ ③ ____________。
(6)定量分析 用电子天平称量得部分数据如下:
玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 | |
反应前 | 28.20 g | 33.00 g | 300.0 g |
反应后 | 32.84 g | 300.4 g |
根据上述数据,纯净的Fe2O3固体质量为_____________g,请选择有效的数据,推断出反应后黑色固体的成分(写出计算过程)__________________________。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:__________________________。