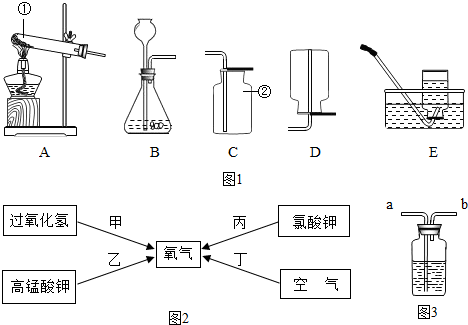
题目内容
在实验室里,甲、乙两同学欲测定碳酸钙样品中碳酸钙的质量分数
(杂质不与酸反应,且受热不分解),分别设计了甲、乙两个实验方案,请回答方案中的问题.甲方案:①称取一定质量的碳酸钙样品;②用酒精灯加热样品,直至质量不再改变
(反应的化学方程式为 );③在干燥的蒸发皿中将固体残留物冷却后称量;④计算.
);③在干燥的蒸发皿中将固体残留物冷却后称量;④计算.
问题
(1)甲为什么要加热样品,直至质量不再改变?问题
(2)甲为什么要将固体残留物放在干燥的蒸发皿中冷却?乙方案:①称取碳酸钙样品
12.5g;②加入质量分数为10%的盐酸73g,使碳酸钙恰好完全反应;③计算.问题
(3)称取样品时,所需的仪器有托盘天平.问题
(4)写出碳酸钙与盐酸反应的化学方程式: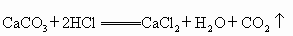
问题
(5)乙方案中,样品碳酸钙的质量分数是80%.综上所述,你认为甲、乙两方案中,切实可行的方案是
_______.不采用另一个方案的原因是__________.
答案:略
解析:
解析:
|
(1) 加热使碳酸钙完全分解(2) 固体残留物温度较高且易吸水.乙方案,不便于操作且实验误差较大. |

练习册系列答案
相关题目