题目内容
铜粉和炭粉的混合物在空气中充分灼烧后,固体的质量没有改变,则原混合物中炭粉的质量分数为
- A.15.8%
- B.20%
- C.80%
- D.84.2%
B
分析:碳在空气中充分灼烧后会燃烧生成二氧化碳气体(碳粉完全消失),铜粉在空气中充分灼烧会生成氧化铜(铜粉质量增加),所以完全灼烧后的固体成分只有氧化铜,根据题意,完全灼烧后得到固体质量与原混合物相同,所以原混合物中碳粉的质量就等于与铜粉发生反应的氧气的质量.
解答:设混合物中碳的质量为X,铜的质量为y,
C+O2 CO2 固体质量减少
CO2 固体质量减少
12 12
x x
2Cu+O2 2CuO 固体质量增加
2CuO 固体质量增加
128 32 32
y
通过题意可知,反应后固体质量不变,
所以x= ,
,
所以原混合物中铜粉与碳粉质量之比为4:1;
则原混合物中铜粉的质量分数为: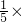 100%=20%,
100%=20%,
故选B.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
分析:碳在空气中充分灼烧后会燃烧生成二氧化碳气体(碳粉完全消失),铜粉在空气中充分灼烧会生成氧化铜(铜粉质量增加),所以完全灼烧后的固体成分只有氧化铜,根据题意,完全灼烧后得到固体质量与原混合物相同,所以原混合物中碳粉的质量就等于与铜粉发生反应的氧气的质量.
解答:设混合物中碳的质量为X,铜的质量为y,
C+O2
 CO2 固体质量减少
CO2 固体质量减少12 12
x x
2Cu+O2
 2CuO 固体质量增加
2CuO 固体质量增加128 32 32
y

通过题意可知,反应后固体质量不变,
所以x=
 ,
,所以原混合物中铜粉与碳粉质量之比为4:1;
则原混合物中铜粉的质量分数为:
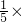 100%=20%,
100%=20%,故选B.
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
将铜粉和炭粉的混合物在空气中充分燃烧后,最终所得黑色物质与原混合物质量相等,则炭粉在原混合物中的质量分数为( )
| A、20% | B、80% | C、15.8% | D、84.2% |
铜粉和炭粉的混合物在空气中充分灼烧后,固体的质量没有改变,则原混合物中炭粉的质量分数为( )
| A、15.8% | B、20% | C、80% | D、84.2% |
铜粉和炭粉的混合物在空气中充分燃烧后,最终得到的黑色物质与原混合物的质量相等,则铜粉和炭粉质量比是( )
| A、1:1 | B、2:1 | C、3:1 | D、4:1 |