题目内容
(2012?黄州区模拟)假期,鲍创同学在家中与妈妈做面包,发现妈妈揉面粉时在面粉中加入一种白色粉末,做出的面包疏松多孔,口感很好.他很感兴趣,想探究这种“神奇粉末”的成分.
通过对市场上相关产品进行调查,鲍创发现了如下图所示的三种商品,
(1)鲍创探究这种白色粉末的成分.
取少量白色粉末于试管中,加入适量蒸馏水,发现白色粉末溶解,无其他明显现象,实验结论是
(2)徐哲同学认为鲍创同学根据上面的实验现象,不能得出白色粉末是纯碱,你若认为徐哲说法有道理,请用化学方程式解释不能得出结沦的原因
根据上面信息,检验白色粉末的方法之一是:20℃时,在100克水中加入12克该白色粉末,充分溶解后,如果有白色固体剩余,则为
(3)在查找资料过程中,鲍创同学还发现纯碱不是碱,是由于其水溶液显碱性而得名.现要验证纯碱溶液是否显碱性,请写出用pH试纸来测其pH值的操作过程
通过对市场上相关产品进行调查,鲍创发现了如下图所示的三种商品,
| 商品 |  |
 |
 |
| 成分 | 碳酸钠 | 碳酸氢钠 | 碳酸氢钠、有机酸 |
取少量白色粉末于试管中,加入适量蒸馏水,发现白色粉末溶解,无其他明显现象,实验结论是
此粉末不是快速发酵粉
此粉末不是快速发酵粉
;另取少量白色粉末于试管中,加入稀盐酸
稀盐酸
,有无色气体产生,鲍创认为白色粉末是纯碱.(2)徐哲同学认为鲍创同学根据上面的实验现象,不能得出白色粉末是纯碱,你若认为徐哲说法有道理,请用化学方程式解释不能得出结沦的原因
NaHCO3+HCl═NaCl+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
.为了得到鉴别纯碱和小苏打的正确方法,鲍创继续查找资料,发现它们有下列的性质| 性质 | 碳酸钠 | 碳酸氢钠 |
| 溶解性 | 20℃时溶解度21.6g,溶解时放热 | 20℃时溶解度9.8g,溶解时放热 |
| 加热 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水. |
碳酸氢钠
碳酸氢钠
.(3)在查找资料过程中,鲍创同学还发现纯碱不是碱,是由于其水溶液显碱性而得名.现要验证纯碱溶液是否显碱性,请写出用pH试纸来测其pH值的操作过程
把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数
把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数
.分析:(1)根据溶解时所出现的现象,结合三种白色粉末的特点,判断粉末是否为快速发酵粉;根据碳酸钠能与盐酸反应放出二氧化碳的特点,推断所加入的试剂;
(2)由于碳酸氢钠也能与盐酸反应放出二氧化碳,可判断滴入盐酸放出二氧化碳的白色粉末也可能是碳酸氢钠;可根据碳酸钠与碳酸氢钠溶解度的不同,由溶解粉末质量的不同,区别两种物质;
(3)根据使用pH试纸测定溶液pH的操作方法.
(2)由于碳酸氢钠也能与盐酸反应放出二氧化碳,可判断滴入盐酸放出二氧化碳的白色粉末也可能是碳酸氢钠;可根据碳酸钠与碳酸氢钠溶解度的不同,由溶解粉末质量的不同,区别两种物质;
(3)根据使用pH试纸测定溶液pH的操作方法.
解答:解:(1)碳酸氢钠能和有机酸反应生成二氧化碳气体,但是该种白色粉末溶解在水中,无明显现象,所以一定不是快速发酵粉,碳酸钠与盐酸反应可放出二氧化碳,因此可推断滴加的试剂应是稀盐酸,故填:此粉末不是快速发酵粉;稀盐酸;
(2)碳酸氢钠与盐酸反应放出二氧化碳,反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑;由于20℃时碳酸钠的溶解度为21.6g而碳酸氢钠的溶解度为9.8g,所以当向100g水中加入12g粉末完全溶解时,粉末为碳酸钠,否则粉末只能为碳酸氢钠,故填:NaHCO3+HCl═NaCl+H2O+CO2↑,碳酸氢钠;
(3)用pH试纸来测溶液pH值的操作过程为:把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数,故填:把一小块试纸放在玻璃片上,用蘸有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数.
(2)碳酸氢钠与盐酸反应放出二氧化碳,反应的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑;由于20℃时碳酸钠的溶解度为21.6g而碳酸氢钠的溶解度为9.8g,所以当向100g水中加入12g粉末完全溶解时,粉末为碳酸钠,否则粉末只能为碳酸氢钠,故填:NaHCO3+HCl═NaCl+H2O+CO2↑,碳酸氢钠;
(3)用pH试纸来测溶液pH值的操作过程为:把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数,故填:把一小块试纸放在玻璃片上,用蘸有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数.
点评:解答本题时要注意到碳酸钠、碳酸氢钠化学性质较为相似,因此常规检验碳酸盐的方法在此问题中存在一定的缺陷,要特别注意.

练习册系列答案
相关题目
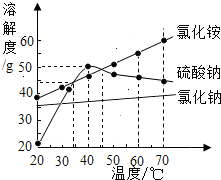 (2012?黄州区模拟)几种物质的溶解度曲线如图.则下列说法正确的是( )
(2012?黄州区模拟)几种物质的溶解度曲线如图.则下列说法正确的是( )