题目内容
【题目】(7分)为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20克于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:
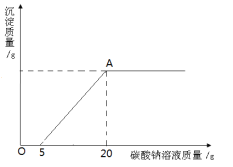
根据题中有关信息和图像分析回答下列问题:
(1)原废液中的溶质成分有 (用化学式回答)。
(2)A点处溶液中溶质的质量是多少克?(通过计算回答)
【答案】(1)HCl 、CaCl2 (2)
【解析】
试题分析:(1)根据反应的图像可知,反应后的溶液中含有盐酸和氯化钙,加入碳酸钠溶液后,碳酸钠先与稀盐酸反应,再与碳酸钠反应生成碳酸钙沉淀和氯化钠;
(2)A点表示碳酸钠与氯化钙恰好完全反应,A点处溶液中溶质是氯化钠,氯化钠来自两个部分:稀盐酸和碳酸钠反应生成的氯化钠和氯化钙与碳酸钠反应生成的氯化钠。利用化学方程式,根据反应的质量比即可计算出生成的氯化钠的质量。
解:设碳酸钠与盐酸反应生成的氯化钠x,碳酸钠与氯化钙反应生成的氯化钠为y
Na2CO3+2HCl= 2NaCl+CO2↑+2H2O Na2CO3+CaCl2= CaCO3↓+ 2NaCl
106 117 106 117
10.6%×5g x 10.6%×15g y
106:117=10.6%×5g: x 106:117=10.6%×15g: y
x=0.585g y=1.755g
故A点处废液中溶质氯化钠的质量为:0.585g+1.755g=2.34g

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目