题目内容
 如图所示,为测定工厂废液中氢氧化钠的含量,小明取25mL加了酚酞视野的废液于锥形瓶中,向其中逐滴加入溶质质量分数为7.3%的稀盐酸,当溶液颜色恰好变为无色时,滴定管中剩余稀盐酸为15mL(所用废液和稀盐酸密度均约为1g/cm3).请计算废液中氢氧化钠的溶质质量分数.
如图所示,为测定工厂废液中氢氧化钠的含量,小明取25mL加了酚酞视野的废液于锥形瓶中,向其中逐滴加入溶质质量分数为7.3%的稀盐酸,当溶液颜色恰好变为无色时,滴定管中剩余稀盐酸为15mL(所用废液和稀盐酸密度均约为1g/cm3).请计算废液中氢氧化钠的溶质质量分数.考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据盐酸的质量求出氢氧化钠的质量,进而求出氢氧化钠溶液的溶质质量分数即可.
解答:解:所用稀盐酸HCl的质量为(25mL-15mL)×1g/mL=10g
含HCl的质量为10g×7.3%=0.73g
设氢氧化钠质量为x
NaOH+HCl=NaCl+H2O
40 36.5
x 0.73g
=
x=0.4g
废液的质量为:25ml×1g/cm3=25g
废液中氢氧化钠的溶质质量分数:
×100%=1.6%
答:废液中氢氧化钠的溶质质量分数为1.6%.
含HCl的质量为10g×7.3%=0.73g
设氢氧化钠质量为x
NaOH+HCl=NaCl+H2O
40 36.5
x 0.73g
| 40 |
| 36.5 |
| x |
| 0.73g |
x=0.4g
废液的质量为:25ml×1g/cm3=25g
废液中氢氧化钠的溶质质量分数:
| 0.4g |
| 25g |
答:废液中氢氧化钠的溶质质量分数为1.6%.
点评:本题主要考查根据化学方程式的计算,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
X、Y、Z三种金属,X在常温下就能与氧气反应,而Y、Z不能;若把Y、Z同时放入硝酸银溶液中时,Y表面有银白色固体析出,而Z表面没明显现象,由实验现象判断,X、Y、Z三种金属的活动性由弱到强的顺序是( )
| A、X Z Y |
| B、Y Z X |
| C、X Y Z |
| D、Z Y X |
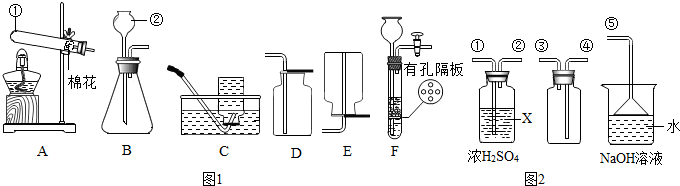
 如图是测定空气里氧气含量的实验装置,请根据实验回答问题:
如图是测定空气里氧气含量的实验装置,请根据实验回答问题: