题目内容
【题目】取24g氢氧化钠和碳酸钠的固体混合物,加136g水完全溶解后,再缓慢加入石灰乳(氢氧化钙和水的混合物)至恰好完全反应,过滤得到4g沉淀和10%的氢氧化钠溶液.试计算反应中应加入石灰乳的质量是多少?
【答案】解:设24g样品中碳酸钠的质量为x,生成的氢氧化钠的质量为y
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
106 100 80
x 4g y![]() ,
, ![]()
x=4.24 g y=3.2 g
得到的10%NaOH溶液的质量为(24g﹣4.24g+3.2g)÷10%=229.6g
加入石灰乳的质量为 229.6 g+4 g﹣136 g﹣24 g=73.6g
答:加入石灰乳的质量为73.6g.
【解析】根据碳酸钠和石灰乳反应产生沉淀碳酸钙的质量4g,可以计算出混合物中的碳酸钠,以及生成的氢氧化钠的质量,根据溶质质量分数的计算公式可以计算出10%的氢氧化钠溶液,根据质量守恒定律进而计算出加入石灰乳的质量.
【考点精析】解答此题的关键在于理解根据化学反应方程式的计算的相关知识,掌握各物质间质量比=系数×相对分子质量之比.

练习册系列答案
相关题目
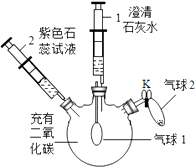
【题目】某同学利用如图装置验证二氧化碳的相关化学性质.
实验装置 | 实验步骤 | 实验现象 |
| ①向外拉注射器1 | 气球1微微鼓起,注射器1中溶液变浑浊 |
②将注射器2中的液体推入瓶中 | 气球1继续微微鼓起,… | |
③打开K,将气球2中的固体氢氧化钠倒入瓶中后,关闭K | 气球1继续变大,… |
(1)步骤①中发生反应的化学方程式是 .
(2)补全步骤②中的现象: .
(3)补全步骤③中的现象: , 其中“气球1继续变大”的原因是 .
(4)通过本实验能验证的二氧化碳的化学性质是 .