题目内容
(每空2分,共10分)空气是一种重要资源,空气质量成为人们日益关注的话题。

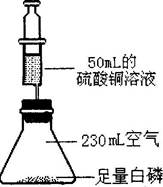
(1)教材中利用上图测定空气中氧气的含量,写出该实验中发生的化学反应方程式 ,实验测得空气中氧气的含量为19.2%,请分析造成该实验出现误差的原因 (列举一项)
(2)某工业城市空气中二氧化碳的含量偏高,其原因是 ,经测定该城市某次降雨的pH约为5,造成该城市空气污染的有害气体主要是 。
(3)为减少空气污染,工业倡导“绿色化学”,其特点之一是实现“零排放”,即反应物的原子全部转化为期望的最终产物.一定条件下,二氧化碳与氢气实现“零排放”反应生成甲酸(HCOOH),参加反应的二氧化碳与氢气的分子个数比为 。

(1)教材中利用上图测定空气中氧气的含量,写出该实验中发生的化学反应方程式 ,实验测得空气中氧气的含量为19.2%,请分析造成该实验出现误差的原因 (列举一项)
(2)某工业城市空气中二氧化碳的含量偏高,其原因是 ,经测定该城市某次降雨的pH约为5,造成该城市空气污染的有害气体主要是 。
(3)为减少空气污染,工业倡导“绿色化学”,其特点之一是实现“零排放”,即反应物的原子全部转化为期望的最终产物.一定条件下,二氧化碳与氢气实现“零排放”反应生成甲酸(HCOOH),参加反应的二氧化碳与氢气的分子个数比为 。
(1)2Cu+O2 2CuO 铜丝的量不足
2CuO 铜丝的量不足
(2)化石燃料的大量燃烧 SO2
(3)1:1
 2CuO 铜丝的量不足
2CuO 铜丝的量不足(2)化石燃料的大量燃烧 SO2
(3)1:1
(1)铜和氧气反应生成氧化铜,根据质量守恒定律知道,反应前后的原子种类和个数都不变,铜和氧气反应的化学方程式为:2Cu+O2 2CuO
2CuO
2CuO,铜丝的量的多少决定了对氧气的消耗量,所以在实验时要保证铜丝过量,实验测得空气中氧气的含量为19.2%<21%,造成该实验出现误差的原因可能是铜丝的量不足;
(2)工业城市中要燃烧大量的化石燃烧煤炭,煤炭燃烧生成大量的二氧化碳和二氧化硫,二氧化硫溶于水生成的亚硫酸能使雨水的pH降低;
(3)一定条件下,二氧化碳与氢气反应生成甲酸(HCOOH),化学方程式为CO2+H2═HCOOH,故参加反应的二氧化碳与氢气的分子个数比为 1:1;
 2CuO
2CuO 2CuO,铜丝的量的多少决定了对氧气的消耗量,所以在实验时要保证铜丝过量,实验测得空气中氧气的含量为19.2%<21%,造成该实验出现误差的原因可能是铜丝的量不足;
(2)工业城市中要燃烧大量的化石燃烧煤炭,煤炭燃烧生成大量的二氧化碳和二氧化硫,二氧化硫溶于水生成的亚硫酸能使雨水的pH降低;
(3)一定条件下,二氧化碳与氢气反应生成甲酸(HCOOH),化学方程式为CO2+H2═HCOOH,故参加反应的二氧化碳与氢气的分子个数比为 1:1;

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目







 MgCl2+ Ca(OH)2== Mg(OH)2 +CaCl2
MgCl2+ Ca(OH)2== Mg(OH)2 +CaCl2