��Ŀ����
����Ŀ����ѧ��ȤС��ͬѧ���ۺ�ʵ������˽��ijʯ�ҳ���һ��ʯ��ʯԭ�ϣ����к��е����ʶ������裨�������費����ˮ�����������ᷴӦ������ʱ�������ֽⷴӦ����Ϊ�˲ⶨ��ʯ��ʯ�Ĵ��ȣ���ȤС��ͬѧȡ��2������ʯ��ʯ��Ʒ����ʵ�������е�δ֪��������������ϡ����20�˷�4�μ��룬��ַ�Ӧ�����ˡ�����Ȳ����������ÿ������������ʣ��������������������ʵ�����ݻ��Ƶ�ͼ���ͼ��
ϡ��������� | ʣ���������� |
��һ�μ���5�� | 1.5�� |
�ڶ��μ���5�� | �� |
�������5�� | 0.5�� |
���Ĵμ���5�� | 0.3�� |
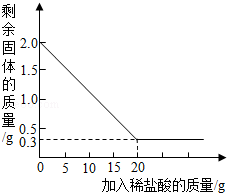
���㣺
��1����������ͼ������ڶ��μ���ϡ�����ʣ������������ �ˣ�
��2����ʯ��ʯ��Ʒ��̼��Ƶ�����������
��3������ϡ���������ʵ����������Ƕ��٣�
���𰸡���1��1.0 ��2��85% ��3��7.3%
��������
����������ɱ������ݿ�֪���ڶ��η�Ӧ��̼���������0.5g��ǰ�����е�ϡ������ȫ��Ӧ����˸���ǰ��������һ�ε����ݿ��Լ�������ϡ���������ʵ�����������
��1����������ͼ������ڶ��μ���ϡ�����ʣ������������1.0g��
��2����ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ��![]() ��100%=85%
��100%=85%
��3���⣺������ϡ���������ʵ���������Ϊx
2HCl+CaCO3=CaCl2+H2O+CO2��
73 100
5x 0.5g
73��100=5x��0.5g
x=7.3%