题目内容
(2008?建邺区一模)下表是元素周期表的一部分| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 第二周期 | 3 Li 锂 7 | 4 Be 铍 9 | 5 B 硼 11 | ① | 7 N 氮 14 | 8 O 氧 16 | 9 F 氟 19 | 10 Ne 氖 20 |
| 第三周期 | 11 Na 钠 23 | ② | 13 Al 铝 27 | 14 Si 硅 28 | ③ | 16 S 硫 32 | 17 Cl 氯 35.5 | 18 Ar 氩 40 |
(2)每个锂原子中的中子数是;正一价锂离子的核外电子数是
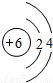
(3)是某元素的原子结构示意图,该元素在上表中的位置是(填①或②或③).
(4)表中②空格处元素应该属于(选填“金属”或“非金属”);其单质的化学活动性比铝(选填“强”或“弱”);该元素形成的氧化物类型为(选填“AO”或“A2O”或“OA”或“A2O3”)
【答案】分析:根据在原子中,原子序数=质子数=核外电子数,相对原子质量=质子数+中子数进行分析解答本题.
解答:解:(1)从元素周期表可查得原子序数为14的元素名称为 硅;从元素周期表可查得相对原子质量为14的元素符号是 N,
故答案为:硅;N;
(2)根据 相对原子质量=质子数+中子数,从元素周期表可查得锂原子的相对原子质量为7,质子数为3,因此,7=3+x,则x=4,所以每个锂原子中的中子数是4;正一价锂离子说明失去一个电子,则 核外电子数是2;
故答案为:4;2;
(3)在原子中,原子序数=质子数=核外电子数,根据某元素的原子结构示意图可知质子数=核外电子数=6=原子序数,因此该元素在上表中的位置是①,
故答案为:①;
(4)根据元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束的规律,表中②空格处元素在钠和铝之间,一定是金属元素,其单质的化学活动性比铝 强,该元素形成的氧化物类型为 AO,
故答案为:金属;AO.
点评:本题考查学生根据在原子中,原子序数=质子数=核外电子数,相对原子质量=质子数+中子数进行分析解题的能力.
解答:解:(1)从元素周期表可查得原子序数为14的元素名称为 硅;从元素周期表可查得相对原子质量为14的元素符号是 N,
故答案为:硅;N;
(2)根据 相对原子质量=质子数+中子数,从元素周期表可查得锂原子的相对原子质量为7,质子数为3,因此,7=3+x,则x=4,所以每个锂原子中的中子数是4;正一价锂离子说明失去一个电子,则 核外电子数是2;
故答案为:4;2;
(3)在原子中,原子序数=质子数=核外电子数,根据某元素的原子结构示意图可知质子数=核外电子数=6=原子序数,因此该元素在上表中的位置是①,
故答案为:①;
(4)根据元素周期表中每一个周期都从金属元素开始,到稀有气体元素结束的规律,表中②空格处元素在钠和铝之间,一定是金属元素,其单质的化学活动性比铝 强,该元素形成的氧化物类型为 AO,
故答案为:金属;AO.
点评:本题考查学生根据在原子中,原子序数=质子数=核外电子数,相对原子质量=质子数+中子数进行分析解题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 (2008?建邺区一模)观察右图标签,回答下列问题
(2008?建邺区一模)观察右图标签,回答下列问题