题目内容
【题目】A、B、C、D、E、F、G、H八种物质存在下图所示关系。其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E、F都是无色液体,H是一种能使澄清石灰水变浑浊的气体。
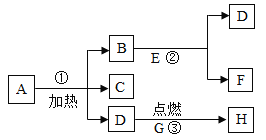
(1)请你根据上述信息,推断出下列物质:E_______,F________。
(2)写出反应②的文字表达式:_______,该反应的基本反应类型为___________。
【答案】二氧化锰 水 过氧化氢![]() 水十氧气 分解反应
水十氧气 分解反应
【解析】
(1)根据A是一种暗紫色固体,加热能生成使带火星的木条复燃的气体D,所以D是氧气,A是高锰酸钾,G在氧气燃烧能生成使澄清的石灰水变浑浊的气体H,所以H是二氧化碳,G是碳,B与无色液体混合能产生氧气,且B在反应前后质量和化学性质都不改变,所以B是二氧化锰,E是过氧化氢,生成的F是水,高锰酸钾分解生成锰酸钾、二氧化锰和氧气,所以C是锰酸钾,经过验证,推出的物质均满足题中的转化关系,推导正确,所以E是过氧化氢,F是水;
(2)反应②是过氧化氢分解制取氧气的反应,其文字表达式为:过氧化氢![]() 水+氧气,该反应符合“一变多”的特征,故是分解反应。
水+氧气,该反应符合“一变多”的特征,故是分解反应。

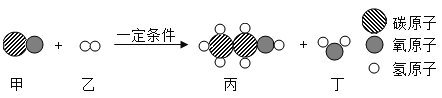
【题目】在一密封容器内,有甲.乙.丙.四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表则下列描述中正确的是
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 20 | m | 8 | 6 |
反应后质量/g | 4 | 待测 | 28 | 2 |
A.待测数值一定为2g
B.乙一定是该反应的催化剂
C.反应中甲和丙的质量比为5:4
D.该反应可能是铜与氧气的反应
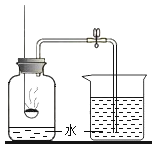
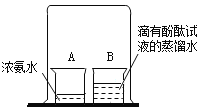
【题目】用对比实验方法探究二氧化碳的性质。
实验一 |
|
(1)装置l中,将Y形导管平放于桌面上,通入CO2后,观察到a管中试纸_____。通过a、b两管中的实验现象说明CO2的性质是_____(用化学方程式表示)。
(2)装置II中,将Y形管固定在铁架台上,a管在上方,b管在下方,缓缓通入CO2后,通过观察到的现象可说明CO2具有①所验证的性质外,还说明CO2的_____。