题目内容
【题目】下面是铁及其化合物的实验探究,请回答相关问题:
(问题Ⅰ)
(1)以赤铁矿为原料冶炼铁的化学反应方程式为____。
(2)将Fe粉溶于稀H2SO4的化学方程式是____,此反应属于____(填基本反应类型)。用点燃法检验生成的H2前必须____。向上述反应后的溶液中滴加NaOH溶液,生成白色Fe(OH)2沉淀,随后沉淀变为灰绿色,白色沉淀变为灰绿色的原因之一是部分Fe(OH)2在湿润的空气中生成Fe(OH)3,其反应的化学方程式____。
(问题Ⅱ)
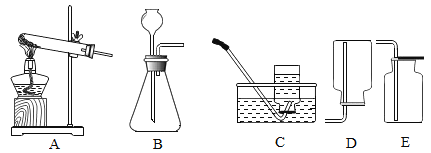
灰绿色固体的热分解实验。过滤、洗涤、低温干燥得到灰绿色固体,其组成为2FeSO42Fe(OH )2Fe2O3[相对分子质量为644]。兴趣小组称取此灰绿色固体6.44g,在科研人员的指导下用下图装置进行热分解实验。
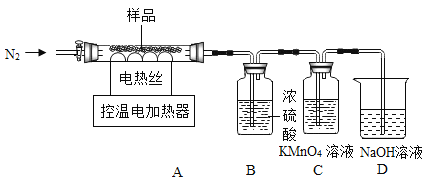
(查阅资料)①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~500℃时完全分解为Fe2O3;
③2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
④浓硫酸只能吸收SO3和H2O。
⑤SO2能使KMnO4溶液褪色
(1)加热前后及过程中均通入N2,加热前通N2的目的是_______。
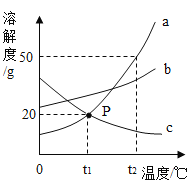
(2)控制温度在不同的范围对A中样品加热,测得剩余固体质量随温度的变化如图所示。

①当加热到t1℃时,装置C中的溶液褪色,则通入到装置C中的气体为____。(填“化学式”)
②图中E点对应的ml=_______。
③图中F点对应物质中Fe2O3的质量为_______g。
④科研人员将F点所得剩余固体隔绝空气,在密闭容器中加热到1400℃,得到纯净的磁性Fe3O4。已知加热过程中发生两个反应,且反应前后固体总质量不变。请写出其中一个反应的化学方程式_______。
【答案】Fe2O3+3CO ![]() 2Fe+3CO2 Fe+H2SO4=FeSO4+H2↑ 置换反应 验纯 4Fe(OH)2+O2+2H2O=4Fe(OH)3 排尽装置中的空气,防止Fe(OH)2被氧化成Fe(OH)3 SO2 6.08(或6.1) 3.20(或3.2) 6Fe2O3
2Fe+3CO2 Fe+H2SO4=FeSO4+H2↑ 置换反应 验纯 4Fe(OH)2+O2+2H2O=4Fe(OH)3 排尽装置中的空气,防止Fe(OH)2被氧化成Fe(OH)3 SO2 6.08(或6.1) 3.20(或3.2) 6Fe2O3![]() 4Fe3O4+O2↑ (或6FeO+O2
4Fe3O4+O2↑ (或6FeO+O2![]() 2Fe3O4)
2Fe3O4)
【解析】
问题Ⅰ:
(1)用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(2)将Fe粉溶于稀H2SO4生成硫酸亚铁和氢气,反应的化学方程式是Fe+H2SO4═FeSO4+H2↑,此反应的反应物是一种单质和一种化合物,生成物是一种单质和一种化合物,属于置换反应;用点燃法检验生成的H2前必须验纯。Fe(OH)2在湿润的空气中与氧气生成Fe(OH)3,其反应的化学方程式是4Fe(OH)2+O2+2H2O═4Fe(OH)3;
问题Ⅱ:
(1)加热前,通入一段时间N2的目的是将装置内的空气排尽,防止氢氧化亚铁被氧化为氢氧化铁;
(2)①当加热到t1℃时,高锰酸钾具有氧化性,能吸收二氧化硫,溶液由紫红色变浅,则通入到装置C中的气体为SO2;
②图2中E点对应的m1为2FeSO42Fe(OH)2Fe2O3中的氢氧化亚铁分解为FeO后剩余固体的质量,
设:生成水的质量为x。

![]() x=0.36g;则m1=6.44g-0.36g=6.08g;
x=0.36g;则m1=6.44g-0.36g=6.08g;
③设:生成Fe2O3的质量为y。
6.44g2FeSO42Fe(OH)2Fe2O3中含有FeSO4的质量=![]() ;
;
6.44g2FeSO42Fe(OH)2Fe2O3中含有Fe2O3的质量=![]() ;
;
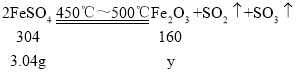
![]() y=1.6g;
y=1.6g;
图2中F点对应物质中Fe2O3的质量为1.6g+1.6g=3.2g;
④F点所得剩余固体是Fe2O3和FeO,隔绝空气,在密闭容器中加热到1400℃,得到纯净的磁性Fe3O4。已知加热过程中发生两个反应,且反应前后固体总质量不变。反应的化学方程式分别为:6Fe2O3![]() 4Fe3O4+O2↑ 和6FeO+O2
4Fe3O4+O2↑ 和6FeO+O2![]() 2Fe3O4。
2Fe3O4。

 阅读快车系列答案
阅读快车系列答案【题目】如图是某同学做“粗盐的提纯”实验时的过滤装置图;
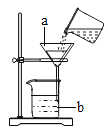
(1)写出标号的仪器名称:a _____,b ___________
(2)图中明显缺少一种玻璃仪器,请写出需要补充的仪器名称是_________,其作用______________。
(3)过滤后的滤液在进行蒸发时也要用到上述补充的仪器,这种仪器在蒸发过程中的作用是_________。
(4)某同学过滤完后发现滤液依然浑浊,除了滤纸可能破损以外,请你再写出一种造成滤液浑浊的原因_____________。
(5)“粗盐的提纯”实验步骤是:称量粗盐 、_________、__________、 __________、称量精盐、计算。称取5.0g粗盐,最终得到4.0g精盐,则精盐的产率是__________。(用百分数表示)
(6)各小组的产率及评价如下:
组别 | 1 | 2 | 3 | 4 |
产率 | 75% | 83% | 88% | 72% |
教师对产率的评价 | 偏低 | 偏高 | 偏高 | 偏低 |
下列各组同学对造成产率偏高或偏低的原因分析,正确的是_____(填编号)。
A第1组:烧杯里的食盐未溶解完就开始过滤
B第2组:蒸发时,有固体物质飞溅
C第3组:滤液浑浊就开始蒸发
D第4组:称量时,精盐中还含有水分
(7)为了鉴别食盐水和蒸馏水,甲同学认为可以用蒸发水分的方法。将所取的两种液体蒸干,留有固体物质的,对应的液体是食盐水;没有固体物质残留的,对应的液体是蒸馏水。他选用的一组仪器是________。
A试管、酒精灯、漏斗、玻璃棒
B酒精灯、蒸发皿、铁架台(带铁圈)、玻璃棒
C托盘天平、酒精灯、量筒、玻璃棒