题目内容
【题目】锌与盐酸(HCl)反应生成氢气和氯化锌。实验室用一定质量的锌与足量盐酸充分反应,生成气体与反应时间关系如图。
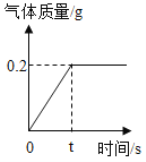
(1)生成氢气的质量为___________g;
(2)参加反应的锌的质量为多少_________?(写出详细计算过程)
(3)充分反应后所得物质中含锌元素的质量为______g。
【答案】0.2 设参加反应的锌的质量为x,则有:
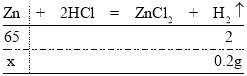
由![]() 解得x=6.5g
解得x=6.5g
答:参加反应的锌的质量为6.5g。 6.5
【解析】
由生成气体与反应时间关系图可知:
(1)生成氢气的质量为0.2g;
(2)设参加反应的锌的质量为x,则有:

由![]() 解得x=6.5g
解得x=6.5g
答:参加反应的锌的质量为6.5g。
(3)根据质量守恒定律充分反应后所得物质中含锌元素的质量为6.5g。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】下表中表示的某系列物质的化学式,根据表格中的内容,下列有关说法正确的是( )
物质序号 | ① | ② | ③ | ④ | …… |
化学式 |
|
|
|
| …… |
A.物质①②③中,氮元素的质量分数从小到大的顺序为①②③
B.若①②两种物质中碳元素的质量相等,则①②两种物质的质量之比为1:2
C.该系列物质的化学式中都有NO2,N(NO2)3中也有,其名称为硝酸氮
D.该系列物质中,某物质所含氮元素的质量分数为11.96%,该物质的化学式为C5H11NO2