题目内容
【题目】实验是进行科学探究的重要手段。请回答下列问题。

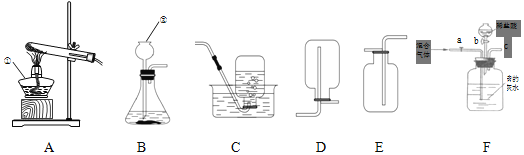
![]() 实验A集气瓶中预先加水的目的是______。
实验A集气瓶中预先加水的目的是______。
![]() 实验中,打开弹簧夹前集气瓶中的实验现象是______,导致测量结果小于
实验中,打开弹簧夹前集气瓶中的实验现象是______,导致测量结果小于![]() 的原因可能是______
的原因可能是______![]() 答一点即可
答一点即可![]() 。
。
![]() 实验C观察到的现象是______,由此说明二氧化碳的性质______。
实验C观察到的现象是______,由此说明二氧化碳的性质______。
![]() 已知:
已知:![]() 和
和![]() 既有相似性,又有差异性。实验D,水槽中滴入紫色石蕊溶液,将收集满两种气体的试管同时倒立于其中,片刻后实验现象如图所示,说明相同条件下的溶解性:
既有相似性,又有差异性。实验D,水槽中滴入紫色石蕊溶液,将收集满两种气体的试管同时倒立于其中,片刻后实验现象如图所示,说明相同条件下的溶解性:![]() ______
______![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() ,试管内溶液变成______色。
,试管内溶液变成______色。
【答案】防止生成的热的熔融物落入集气瓶底,炸裂集气瓶 红磷燃烧,产生大量白烟 红磷量不足![]() 或装置气密性不好或未完全冷却就打开弹簧夹
或装置气密性不好或未完全冷却就打开弹簧夹![]() 蜡烛由低到高依次熄灭 二氧化碳密度大于空气,且二氧化碳不燃烧也不支持燃烧
蜡烛由低到高依次熄灭 二氧化碳密度大于空气,且二氧化碳不燃烧也不支持燃烧 ![]() 红
红
【解析】
(1)实验A铁丝在氧气中燃烧有高温熔融物生成,集气瓶中预先加水的目的是防止生成的热的熔融物落入集气瓶底,炸裂集气瓶;
(2)B实验中,打开弹簧夹前集气瓶中的实验现象红磷燃烧,产生大量白烟,导致测量结果小于五分之一的原因可能是红磷量不足(或装置气密性不好或未完全冷却就打开弹簧夹);
(3)向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是:不能燃烧、不能支持燃烧且密度比空气的大,因此,二氧化碳可用于灭火;
(4)根据图示可以看出,二氧化硫的这支试管内液面上升的明显,故二氧化硫的溶解性强于二氧化碳,二氧化硫的水溶液呈酸性,能使石蕊试液变成红色。

【题目】某课外小组用大理石与盐酸反应制取二氧化碳(大理石中杂质不与盐酸反应)。
甲同学进行实验,实验数据如下(烧杯的质量为25.0g)
烧杯+盐酸 | 大理石 | 充分反应后烧杯+剩余物 | |
甲 | 75.0g | 13.2g | 83.8g |
所取的大理石和盐酸恰好完全反应,请回答下列问题:
(1)实验中产生的二氧化碳的质量为_____。
(2)计算大理石中碳酸钙的质量分数_____(计算结果精确到01%)。