题目内容
如图为某化工企业生产流程示意图:下列说法正确的是( )
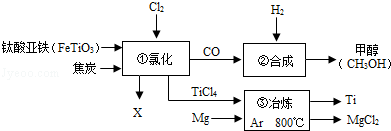

| A.钛酸亚铁(FeTiO3)中钛元素为+3价 |
| B.③中氩气(Ar)作反应物,反应类型为置换反应 |
| C.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 |
D.①中反应为:2FeTiO3+6C+7Cl2 2X+2TiCl4+6CO,则X为FeCl3 2X+2TiCl4+6CO,则X为FeCl3 |
D
试题分析:A、根据在化合物中元素化合价的代数和为零的原则,设钛元素的化合价为a,则(+2)+a+(﹣2)×3=0,a=+4,故A错;B、因为镁的化学性质活泼,故用镁和氯化钛冶炼钛时需要氩气做保护气,氩气(Ar)作反应物是错误的,反应类型是置换反应,故C错;
C、一氧化碳和氢气反应生成甲醇的化学方程式为CO+2H2═CH3OH;一氧化碳与氢气的质量比为28:4=7:1,故C错;
D、根据质量守恒定律,化学反应前后原子的种类和个数不变,反应前Fe:2,Ti:2,O:6,C:6,Cl:14;反应后Fe:0,Ti:2,O:6,C:6,Cl:8;故2X中含有2个铁原子,6个氯原子,故X的化学式为:FeCl3;故D正确.

练习册系列答案
相关题目