题目内容
【题目】有一包黑色粉末,可能由C、CuO、Fe三种物质中的一种或几种组成。某化学兴趣小组为了探究它的成分,按如下步骤进行实验。
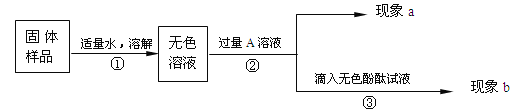
(1)先对实验做了如下设想和分析:黑粉中只有碳粉不溶解于稀盐酸。取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况)。请你完成下表。
烧杯中可能出现的现象 | 结论 |
① | 只含C |
②固体部分溶解,溶液变成蓝色,无气泡 | |
③有黑色不溶物,有气泡逸出,溶液呈浅绿色 | 含C、Fe |
(2)通过实验及分析,确定该粉末为C、CuO的混合物。为了进一步探究C、CuO的性质,他们又利用这种混合物补充做了下面两个实验。
【实验一】将此粉末敞口在空气中灼烧完全,待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。烧杯中 (填“有”或“无”)不溶物,溶液呈 色。
【实验二】将此粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请回答:①烧杯中 (填“有”或“无”)不溶物;②若静置后溶液呈无色,则该溶液中溶质是 (写化学式);③若静置后溶液呈蓝色,该实验过程中所发生反应的化学方程式 、 。
【答案】
固体不溶解,无气泡,溶液颜色无变化 | |
含C和CuO | |
【实验一】无 蓝
【实验二】有 H2SO4 2CuO+C![]() 2Cu+CO2↑ CuO+ H2SO4=CuSO4+H2O
2Cu+CO2↑ CuO+ H2SO4=CuSO4+H2O
【解析】
试题分析:氧化铜能与酸反应生成蓝色溶液,铁能与酸反应生成气体,碳不能与酸反应。根据三种物质的性质,若只含有碳,那么固体不溶解,无气泡,溶液颜色无变化;若固体部分溶解,溶液变成蓝色,无气泡说明含有碳和氧化铜;若有黑色不溶物,有气泡逸出,溶液呈浅绿色,那么含有碳和铁;若固体全部溶解,溶液变成蓝色,无气泡产生那么只含有氧化铜。
【实验一】:因为碳可以与氧气反应生成二氧化碳气体,所以将此粉末在空气中灼烧完全后,剩余的固体是氧化铜,它可以与稀硫酸反应,生成蓝色的硫酸铜溶液;
【实验二】:①因为碳单质具有还原性,可以将氧化铜还原为红色的铜,所以将此粉末隔绝空气加热后,剩余的固体是Cu,而Cu不与稀硫酸反应;
②若静置后溶液无色,则说明氧化铜被全部还原,则溶质为硫酸;
③若静置后溶液呈蓝色,则说明还存在着氧化铜,故发生的反应为:氧化铜与碳,及氧化铜和硫酸的反应。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案【题目】除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作都正确的是
选 项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A | CaO(CaCO3) | 足量的水 | 溶解、过滤、蒸发 |
B | N2(O2) | 木炭 | 通过灼热的木炭 |
C | NaCl(NaOH) | 过量稀盐酸 | 溶解、蒸发 |
D | MnO2(KCl) | 水 | 溶解、过滤、洗涤、烘干 |