题目内容
【题目】甲、乙、丙三种物质的溶解度曲线如图所示,但不知它们分别对应哪条曲线。
已知:①甲和乙不可能配制成相同浓度的饱和溶液
②甲和丙中有一种物质,其接近饱和的溶液可通过升温达到饱和
③将t3℃时三种物质的饱和溶液降温到t1℃,乙的溶质质量分数大于丙根据上面信息,回答下列问题:
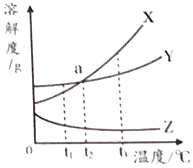
(1)曲线Z代表______(填“甲”、“乙”或“内”)。
(2)t1℃时,三种物质的溶解度大小为______。
(3)结合题意,下列说法正确的是______。
a.t3℃时,等质量的甲、乙、丙饱和溶液中,甲的溶质质量分数最小
b.将t3℃时等质量乙和丙的饱和溶液降温到t2℃时,所得溶液的溶质质量分数相同
c.t3℃时,分别将乙和丙的饱和溶液降温至t1℃,丙析出的晶体一定比乙多
d.改变同一条件可以使甲、乙、丙不饱和溶液变为饱和溶液
【答案】甲 乙>丙>甲 ad
【解析】
根据题目信息和溶解度曲线可知:甲和乙不可能配制成相同浓度的饱和溶液;说明甲和乙有一个是Z物质;甲和丙中有一种物质,其接近饱和的溶液可通过升温达到饱和,说明甲是Z;将t3℃三种物质的饱和溶液降温到t1℃,乙的溶质质量分数大于丙,说明乙是Y,丙是X。
(1)根据分析可知Z代表甲;
(2)根据溶解度曲线可知:t1℃时,三种物质的溶解度大小为Y>X>Z,即乙>丙>甲;
(3)a、t3℃时,甲物质的溶解度最小,所以等质量的甲、乙、丙饱和溶液中,甲的溶质质量分数最小,故选项正确;
b、对于相同质量的乙和丙,溶解度越大,溶剂质量越小,即乙的溶剂质量小于丙,乙和丙的溶解度均随温度的降低而降低,在t2℃时,它们仍为饱和溶液,此时两者的溶解度相同,故乙的质量分数大于丙,故选项错误;
c、因为没有指出两种溶液的总质量,故t3℃时,分别将乙和丙的饱和溶液降温至t1℃,丙析出的晶体不一定比乙多,故选项错误;
d、通过减少溶剂的质量可以使甲、乙、丙不饱和溶液变为饱和溶液,故选项正确。故选ad。

 小学课时特训系列答案
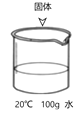
小学课时特训系列答案【题目】已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g.
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
固体的质量/g | 30 | 60 | 30 | 60 | 90 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
下列关于①-⑤实验操作所得溶液说法不正确的是
A. 溶质质量:①<②B. 溶液质量:②<④C. 溶质质量分数:①=③D. ⑤中溶液质量:190g
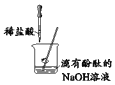
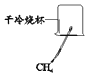
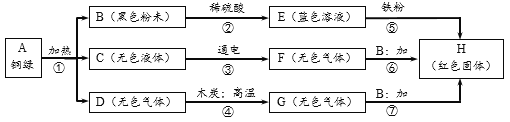
【题目】根据下图所示实验,能达到实验目的是( )
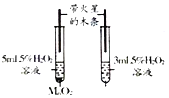
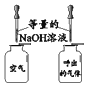
A.证明稀盐酸与 NaOH反应 | B.检验CH4燃烧生成CO2和H2O | C.证明MnO2的催化作用 | D.比较呼出气体和空气中CO2的含量 |
|
|
|
|
A. AB. BC. CD. D