题目内容
【题目】某兴趣小组回收实验室制CO2的废液,重新制得CaCO3和NaCl晶体,过程如下:
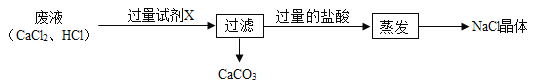
(1)试剂X为什么要过量___?
(2)过量的盐酸对所得到NaCl晶体的纯度有没有影响___?请说明原因______。
【答案】用过量的碳酸钠除去溶液中钙离子和氢离子 否 蒸发结晶氯化钠溶液时,受热后的稀盐酸会变为氯化氢气体被排出,不会影响氯化钠的纯度
【解析】
混合废液中加入试剂X过滤后能产生碳酸钙,则试剂X中含有碳酸根离子,滤液中加入过量的稀盐酸,蒸发后能产生氯化钠晶体,则试剂X中的阳离子是钠离子,则试剂X是碳酸钠;
(1)过量的碳酸钠能与稀盐酸反应产生氯化钠和水和二氧化碳,能与氯化钙反应产生碳酸钙沉淀和氯化钠,用过量的碳酸钠除去溶液中钙离子和氢离子;
(2)过量的盐酸对所得到NaCl晶体的纯度没有影响,因为蒸发结晶氯化钠溶液时,受热后的稀盐酸会变为氯化氢气体被排出,不会影响氯化钠的纯度。

练习册系列答案
相关题目