题目内容
【题目】某校化学兴趣小组就空气中氧气的含量进行实验探究,请你参与。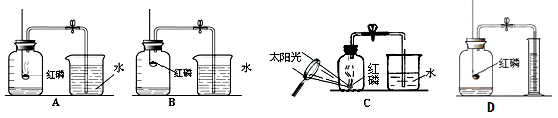
(1)【设计实验】第一小组同学共同设计了如上图的A、B两套装置。 你认为合理的是(填编号)。
(2)【进行实验】
【数据分析】 实验结束后,整理数据如下:(注:集气瓶容积为100ml)
组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入瓶中水的体积(ml) | 20 | 18 | 19 | 17 | 21 | 19 |
通过对实验数据分析,实验得出氧气约占空气体积的。
(3)【实验分析】红磷要足量的原因是;
(4)发生反应的化学方程式是;
(5)实验结束,发现测定出的空气中氧气的体积分数低于l/5,可能的原因是
①可能使用红磷的量不足,瓶内氧气没有消耗完
②可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
③可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
④可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
(6)【改进实验】
①第二小组同学设计了C实验装置,优点是:。
②第三小组同学设计了D实验装置,优点是:。
【答案】
(1)A
(2)五分之一
(3)可充分消耗的氧气,使测量的结果更准确
(4)4P+5O2 ![]() 2P2O5
2P2O5
(5)①③
(6)环保.同时也利于实验的结果的准确,方便、准确计算进入集气瓶中水的体积
【解析】本题考查测定氧气在空气中的体积分数,实验中要注意装置的严密性、所用药品的量、生成物的状态、氧气不足1/5的误差分析、对实验现象的分析等。
【设计实验】实验A和B的区别在于红磷的位置,而这一点与氧气的密度有关,由于氧气的密度大于空气,所以红磷在稍微低的位置更利于反应的进行,也更利于氧气的消耗,所以实验设计A更合理;
【数据分析】根据集气瓶的容积是100ml,进入水的量的几次不同结果求其平均值可得:进入水量的平均值是19ml,所以进入水量占总容积的19%,即氧气量约占空气体积的五分之一;
【实验分析】:(1)红磷足量可充分消耗的氧气,使测量的结果更准确;(2)红磷燃烧的化学方程式为:4P+5O2 ![]() 2P2O5(3)①实验中所取红磷的量不足时,会导致装置内氧气不能全部消耗,因此使测得氧气的体积分数会小于的
2P2O5(3)①实验中所取红磷的量不足时,会导致装置内氧气不能全部消耗,因此使测得氧气的体积分数会小于的 ![]() ;②实验前若没有将弹簧夹夹紧,会导致实验中装置内的气体受热膨胀而逸出,因此测得氧气的体积分数会大于
;②实验前若没有将弹簧夹夹紧,会导致实验中装置内的气体受热膨胀而逸出,因此测得氧气的体积分数会大于 ![]() 的;③未塞紧瓶塞,冷却时会使空气进入集气瓶内,因此测得氧气的体积分数小于的
的;③未塞紧瓶塞,冷却时会使空气进入集气瓶内,因此测得氧气的体积分数小于的 ![]() ;④插入燃烧匙太慢,塞紧瓶塞之前,瓶内的部分空气受热逸出,因此测定氧气体积分数大于的
;④插入燃烧匙太慢,塞紧瓶塞之前,瓶内的部分空气受热逸出,因此测定氧气体积分数大于的 ![]() ;综上所述就选①③
;综上所述就选①③
【改进实验】:(1)实验C是在装置内点燃,生成的五氧化二磷不会跑到空气中,也就是红磷燃烧的产物有毒的五氧化二磷不会散失到空气造成环境污染,节约了红磷,故C装置的优点是:环保.同时也利于实验的结果的准确.(2)采用量筒进行实验的优点是方便、准确计算进入集气瓶中水的体积。
【考点精析】利用书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知注意:a、配平 b、条件 c、箭号.

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案