题目内容
【题目】请结合下图回答问题:
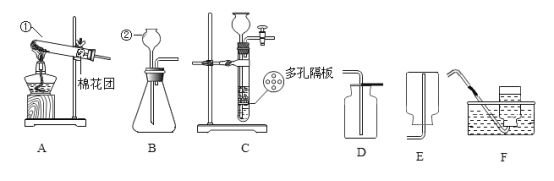
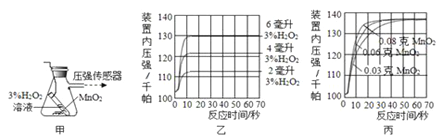
(1)写出图中有标号仪器的名称:①_____,②_____,装置A、B、C是常见的气体发生装置,根据_____,可将其分成两类.
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是(填字母编号,下同)_____,收集一瓶干燥的氧气可以选用装置_____。
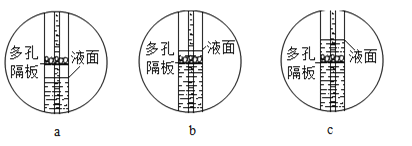
(3)如图,是在运用C装置制取气体时遇到的情景.当液面变化按照_____(填序号)顺序时,导管上的活塞是在_____状态(填“打开”或“关闭”),此时停止了气体的制取。
(4)选用F装置收集气体时,下列实验操作的正确顺序为_____(填序号).
①等到气泡连续且均匀时,再将导管口移入集气瓶
②将集气瓶盖上玻璃片再移出水槽
③将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
(5)用一定量20%的过氧化氢溶液和二氧化锰制氧气,应选用的发生装置是_____,写出该反应的符号表达式_____,制取过程中,同学们发现不能得到平稳的氧气流.大家提出从两个方面加以改进:一是控制液体的滴加速度,_____,二是_____。
(6)某化学小组研究能使带火星木条复燃时氧气的最低含量,他们在集气瓶中装入不同体积的水,用排水法收集氧气。当发现在瓶中最少放入35%的水时,收集到氧气就可以使带火星的木条复燃,这时集气瓶中氧气的体积分数是_____(计算精确到0.1%)
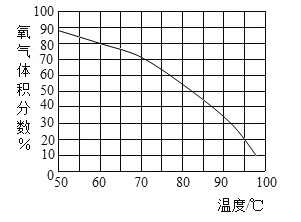
用带火星的木条直接检验双氧水受热分解产生的氧气时,往往难以复燃,这是因为_____所致,此时混合气体中氧气的体积分数随温度变化的曲线如图所示.若只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,应将加热双氧水的最高温度控制在_____°C以下。
【答案】试管 长颈漏斗 药品的状态和反应条件 A D cba 关闭 ③①② B 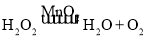 把发生装置的长颈漏斗改为分液漏斗(或注射器) 将过氧化氢溶液加水稀释 48.7% 加入双氧水时,溶液中水蒸气随氧气一起逸出,环境湿度大,氧气的含量较少 83
把发生装置的长颈漏斗改为分液漏斗(或注射器) 将过氧化氢溶液加水稀释 48.7% 加入双氧水时,溶液中水蒸气随氧气一起逸出,环境湿度大,氧气的含量较少 83
【解析】
高锰酸钾加热生成锰酸钾、二氧化锰和氧气,过氧化氢在二氧化锰催化作用下生成水和氧气。
(1)图中有标号仪器的名称:①是试管,②是长颈漏斗,装置A是固体加热装置,B、C是固液制取装置,常见的气体发生装置,根据药品的状态和反应条件,可将其分成两类。
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,用加热高锰酸钾的方法制取氧气,应选用的发生装置是A,收集一瓶干燥的氧气,用向上排空气法收集,故选用装置D。
(3)固体物质在多孔塑料隔板上,当反应进行时隔板上的固体与液体接触,反应进行;当把止水夹关闭时,产生的气体是压强增大,把液体压入长颈漏斗,隔板上的固体与液体分离,反应停止,运用C装置制取气体时遇到的情景,是物质在反应,压强变大,当液面变化按照cba顺序时,导管上的活塞是在关闭状态,此时停止了气体的制取。
(4)选用F装置收集气体时,下列实验操作的正确顺序为将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中,等到气泡连续且均匀时,再将导管口移入集气瓶,将集气瓶盖上玻璃片再移出水槽,故正确顺序为③①②。
(5)过氧化氢在二氧化锰催化作用下生成水和氧气,故应选用的发生装置是B,反应的符号表达式为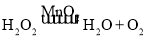 ,制取过程中,不能得到平稳的氧气流,改进方法:一是控制液体的滴加速度,把发生装置的长颈漏斗改为分液漏斗(或注射器),二是将过氧化氢溶液加水稀释。
,制取过程中,不能得到平稳的氧气流,改进方法:一是控制液体的滴加速度,把发生装置的长颈漏斗改为分液漏斗(或注射器),二是将过氧化氢溶液加水稀释。
(6)瓶中最少放入35%的水,空气的体积为![]() ,空气中氧气的体积分数为
,空气中氧气的体积分数为
![]() ,集气瓶中氧气的体积分数是
,集气瓶中氧气的体积分数是![]()
用带火星的木条直接检验双氧水受热分解产生的氧气时,往往难以复燃,这是因为加入双氧水时,溶液中水蒸气随氧气一起逸出,环境湿度大,氧气的含量较少。若只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,应将加热双氧水的最高温度控制在83°C以下。

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案【题目】某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
①称取1.6g胆矾(CuSO4·5H2O)晶体,研细后加入10mL蒸馏水溶解。
②将足量的NaOH溶液与上述溶液充分反应生成蓝色沉淀,过滤后洗涤沉淀。
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变黑色,研细备用。
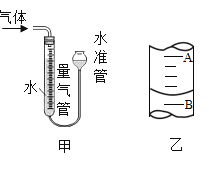
④按上表中的质量混合好固体后,在相同条件下加热试管并与(MnO2)的催化效果做比较,实验时间均以生成50mL气体为准(见图甲),其他可能影响实验甲乙的因素均忽略。回答下列问题:
编号 | 氯酸钾(KClO3)质量/g | 其他物质质量/g | 待测数据 |
1 | 2 | / | |
2 | 2 | 氧化铜(CuO)0.5 | |
3 | 2 | 二氧化锰(MnO2)0.5 |
(1)上述实验步骤中需要使用玻璃棒的是__________。(填序号)
(2)表格中“待测数据”是指________。
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意_________
a 视线与凹液面最低处相平
b 读数前不能移动量气管和水准管
c 保持水准管静止,待水准管中液面不再上升时,立刻读数
d 读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差lmL,刻度A为20,则此时气体的读数为___________。
(5)如果要进一步探究(CuO)在反应中是否起到催化作用,请完成后续实验。(提示:可从催化剂的概念完成实验)
实验步骤 | 设计这一步骤的目的 |
实验表明,加入氧化铜(CuO)后产生氧气(O2)的速率比未加入时快得多 | 氧化铜(CuO)能加快氯酸钾(KClO3)的分解 |
①___________ | ___________ |
②___________ | ___________ |