题目内容
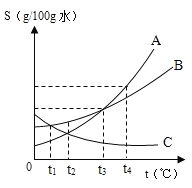
【题目】下图是A、B、C三种固体的溶解度曲线,请据图回答下列问题:
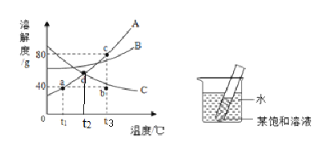
(1)d点所表示的意义是_______,t1°C时,A、B、C三种物质的溶解度大小顺序为_____
(2)t3°C时,30gA物质加入到50 g水中不断搅拌,所得溶液溶质质量分数为_____(保留到0.1%)
(3)t3℃时,相同质量的A、B、C三种物质的饱和溶液降温至t1°C,析出晶体最多的是_____,此时三种物质的溶液的溶质质量分数由大到小的顺序是________。
(4)如图所示,试管内装有A、B、C三种物质之一的饱和溶液,向烧杯中的水中加入氢氧化钠固体,试管中有晶体析出。由此判断试管内的溶液是________(填字母序号)物质的溶液。
(5)某同学在实验室用固体B和蒸馏水配制50 g质量分数为6%的B溶液时,涉及以下实验步骤:① 溶解② 称量和量取③ 计算④ 装入试剂瓶贴好标签。配制上述溶液正确的实验步骤顺序是____________(填序号)。
【答案】t2°C时,AC两物质的溶解度相同 C>B>A 37.5% A B>C>A C ③②①④
【解析】
(1)在溶解度曲线图上,横坐标是温度,纵坐标是溶解度,d点所表示的意义是t2°C时,AC两物质的溶解度相同,t1°C时,A、B、C三种物质的溶解度大小顺序为C>B>A;
(2)由图中信息可知,t3°C时,A的溶解度为80g,即100g水中最多可溶80gA,30gA物质加入到50 g水中不断搅拌,溶质为30g,溶液80g,所得溶液溶质质量分数为:30g÷80g×100%=37.5%; ![]()
(3)t3℃时,相同质量的A、B、C三种物质的饱和溶液降温至t1°C,由于A的溶解度较小的最多,析出晶体最多的是A,![]() ,降温后A、B得t1°C时饱和溶液,由于此时B的溶解度比A的大,B的饱和溶液质量分数比A的大,降温时C的溶解度变大,溶质不析出,溶质的质量分数与t3℃时的饱和溶液溶质的质量分数相同,而C在t3℃时的溶解度大于t1°C时A的溶解度而小于B,所得溶液溶质的质量分数比A大、比B小,在此时三种物质的溶液的溶质质量分数由大到小的顺序是B>C>A;
,降温后A、B得t1°C时饱和溶液,由于此时B的溶解度比A的大,B的饱和溶液质量分数比A的大,降温时C的溶解度变大,溶质不析出,溶质的质量分数与t3℃时的饱和溶液溶质的质量分数相同,而C在t3℃时的溶解度大于t1°C时A的溶解度而小于B,所得溶液溶质的质量分数比A大、比B小,在此时三种物质的溶液的溶质质量分数由大到小的顺序是B>C>A;
(4)如图所示,试管内装有A、B、C三种物质之一的饱和溶液,向烧杯中的水中加入氢氧化钠固体,氢氧化钠溶于水放出大量热,溶液温度升高,试管中有晶体析出。说明试管内溶质的溶解度随温度升高而减小,由此判断试管内的溶液是C物质的溶液;
(5)配制一定溶质质量分数的溶液的操作步骤是:计算、称量、溶解、装瓶存放,某同学在实验室用固体B和蒸馏水配制50 g质量分数为6%的B溶液时,涉及以下实验步骤:① 溶解② 称量和量取③ 计算④ 装入试剂瓶贴好标签。配制上述溶液正确的实验步骤顺序是③②①④。

 阅读快车系列答案
阅读快车系列答案