��Ŀ����
����Ŀ�������������������䡰ʽ�������жϣ��ټ�ʽ����ƵĻ�ѧʽΪCa4(OH)(PO4)3����Fe3O4�ɿ�������������ʱ�ɸ�д��FeOFe2O3�����ݻ��ϼ۹��ɺ�ǰ��д������Pb3O4����������Ǧ���ɸ�дΪ2PbOPbO2(Pb�Ļ��ϼ�Ϊ+2�ۡ�+4�ۣ�����Ϊ�˷���ijЩ��ѧ���㣬98%��ŨH2SO4��дΪ9H2SO4H2O���д������
A. ֻ�Т� B. ֻ�Т� C. �٢� D. �ڢ�
���𰸡�D
��������
����Ca4(OH)(PO4)3�У���Ԫ��Ϊ+2�ۡ�������Ϊ��1�ۡ������Ϊ��3�ۣ��仯�ϼ۴�����Ϊ����+2����4+����1��+����3����3����2��0���ʢٴ���
��Fe3O4�ɿ�������������ʱ�ɸ�д��FeOFe2O3��FeO��Fe2O3�ֱ���Ԫ��+2�ۡ�+3��������Ļ�ѧʽ��Pb�ڻ���������+2�ۺ�+4�ۣ����ݻ��ϼ۴�����Ϊ���ԭ��Pb��+2�ۺ�+4��������������ʽΪPbO��PbO2����Pb3O4��������ı�ʾ��ʽ����д�� 2PbOPbO2���ʢ���ȷ��
��98%��Ũ������������ˮ�������ȣ�98��2�������Һ��������ˮ�ķ��Ӹ�����= ![]() ����98%��Ũ����ɸ�д��9H2SO4H2O���ʢ���ȷ���ʢڢ�˵����ȷ����ѡD��
����98%��Ũ����ɸ�д��9H2SO4H2O���ʢ���ȷ���ʢڢ�˵����ȷ����ѡD��

����Ŀ����ѧ����ʵ��Ϊ�����Ŀ�ѧ��������ѧʵ��֪ʶ�ش��������⣺

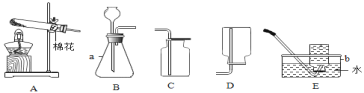
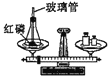
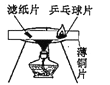
��1���о���ȼ��ȼ�յ���������֪�������Ż����40�档����ͼ��ʾװ�ý���ʵ�飺����ƿ�ڼ���80�����ҵ���ˮ�պ�û��ȼ�ճ��еİ��ף�����ע������ƿ�����������ƿ��ˮ���½���������¶��ˮ��ʱ����ȼ�ա�
�ٰ���ȼ��ʱ������Ӧ�Ļ�ѧ����ʽΪ_________________________��
�ڴ�ʵ���о���ȼ��ȼ�յ�������_________________________��
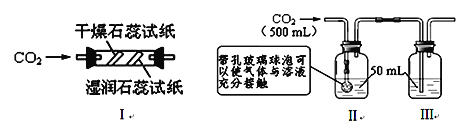
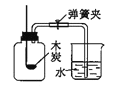
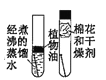
��2�����ñ���װ�ý��ж�����̼���ʵ�ʵ�顣ʵ��ǰֹˮ�д��ڹر�״̬��
ʵ��װ�� | ʵ��1 | ʵ��2 |
| ��. ��A�Թܳ���CO2��B�Թܼ�����ɫʯ����Һ ��. �ܱ��£�����Ͳ��A�в���CO2��� ��. ��K | ��. ��A�Թܳ���CO2��B�Թܼ���ϡ���� ��. ����Ͳ��A ��ע�������ı��ͳ���ʯ��ˮ���� ��. ��K |
��ʵ��1�У�������֤CO2��ˮ������Ӧ��������������______________________��
��ʵ��2�У�������з�����Ӧ�Ļ�ѧ����ʽΪ____________________________��������У���K����A��Һ��____________________�������ݲ�����
����Ŀ����һ���ܱ������з���A��B��C��D�������ʣ���һ�������·�����ѧ��Ӧ��һ��ʱ�����й��������£�
���� | A | B | C | D |
��Ӧǰ���� (g) | 9 | 2 | 22 | 1 |
��Ӧ������(g) | x | 2 | 6 | 21 |
(1)��һ��Ӧ�� x=________g��
(2)д��һ����������Ӧ������ͬ�Ļ�ѧ����ʽ��_________��