题目内容
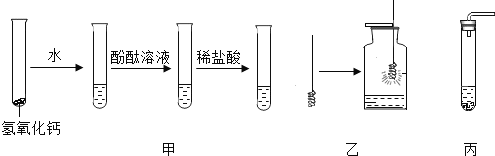
【题目】某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质的质量分数。
实验一:37%的浓盐酸(密度为1.19g/mL)、氢氧化钠溶液、蒸馏水、量筒、细口瓶等
实验步骤:
(1)计算:配制74g质量分数为10%的稀盐酸,需要37%的浓盐酸的体积为 mL(精确到0.1mL,下同);需要蒸馏水的体积为 mL(水的密度为1.0g/mL)。

(2)量取:用量筒分别量取相应的浓盐酸和蒸馏水。
(3) 。
(4)装瓶并贴上标签。
实验二:用上述配制的稀盐酸加入到20g某氢氧化钠溶液中,溶液pH的变化情况如右图所示。试计算该氢氧化钠溶液中溶质的质量分数。 (在答题卡上写出计算过程)
【答案】实验步骤:(1)16.8 54.0 (3) 混和均匀 (4)20%
【解析】
试题分析:配制74g质量分数为10%的稀盐酸,需要37%的浓盐酸的体积为X,则74克×10%=X×1.19g/mL×37%,解得X=16.8ml,需要蒸馏水的体积为74mL-16.8ml×1.19g/mL=54ml。量取:用量筒分别量取相应的浓盐酸和蒸馏水,然后混合均匀即成为要配制的溶液。
解:设参加反应的氢氧化钠溶液中溶质的质量为x。
NaOH + HCl = NaCl + H2O
0 36.5
x 36.5 g×10%
40:36.5= x:36.5 g×10%
x = 4g
氢氧化钠溶液中溶质的质量分数为4g/20g×100%=20%

练习册系列答案
相关题目