题目内容
盐水选种是我国古代劳动人民发明的一种巧妙的挑选种子的方法.农业生产上常用质量分数15%——20%的氯化钠溶液来选种.为了测定某氯化钠溶液是否符合要求,取该溶液70g,加入一定溶质质量分数的AgNO3溶液100g,恰好完全反应【已知:氯化钠溶液和硝酸银溶液反应生成氯化银(AgCl)沉淀和硝酸钠】.过滤分离出沉淀的质量为28.7g.
(1)反应后所得溶液的质量为 g.
(2)通过计算确定该氯化钠溶液是否符合选种要求?(计算结果精确到0.1%)
(1)141.3; (2)16.7%,符合要求
解析试题分析:(1)反应后所得溶液的质量=70g+100g﹣28.7g=141.3g;故填:141.3;
(2)解:设该氯化钠溶液中氯化钠的质量为X.
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
X 28.7g =
=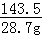
X=11.7g
溶液中氯化钠的质量分数=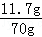 ×100%=16.7%
×100%=16.7%
15%<16.7%<20%,符合要求
答:该氯化钠溶液符合选种要求.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.
点评:本题主要考查了根据化学方程式计算有关物质的质量和有关溶质质量分数的计算,培养学生的分析问题、解决问题的能力,难度较大.

练习册系列答案
相关题目
某钢铁厂需要测定一批生锈较严重的废钢材的锈蚀程度(假定该废钢成分为铁、氧化铁和杂质,杂质不溶于水不发生任何反应,而硫酸先与氧化铁反应),取该样品28g加入一洁净的烧杯中,再将足量的250克稀硫酸平均分为5次加入到烧杯中,获得实验数据如下:
| 稀硫酸质量(单位/g) | 50 | 50 | 50 | 50 | 50 |
| 烧杯内剩余物质总质量(单位/g) | 78 | 128 | 178 | 227.8 | 277.6 |
将烧杯内物质过滤得到滤液276.8g,试回答下列问题:(注:该题用初中知识解答)
(1)上述过程中生成气体的化学方程式为: ;
(2)共生成气体的质量是 ;
(3)根据已知条件列出求解参加反应的单质铁的质量(x)的比例式 ;
(4)所用稀硫酸的溶质质量分数是 ;
(5)该样品中被锈蚀的铁元素占原钢材(被锈蚀前的)的质量分数为 。(取整数)
如图是某试剂瓶标签上的内容.
| 浓硫酸(分析纯) 化学式:H2SO4相对分子质量:98 密度:1.84g∕cm3质量分数;98% |
(1)把这种浓硫酸稀释为溶质质量分数是19.6%的硫酸溶液100g,需要这种硫酸的质量为
(2)将稀释后的硫酸溶液与200g氢氧化钠溶液恰好完全反应,求氢氧化钠溶液的溶质质量分数.