题目内容
某兴趣小组在实验室中用氯酸钾制取氧气,实验测得相关数据如下图所示:
(1)反应生成氧气质量为 g。
(2)计算剩余的混合物中二氧化锰的质量(计算结果保留二位小数)。
(1)氧气的质量为4.8 g(1分)
(2)4.75g
解析试题分析:化学反应应遵守质量守恒定律,参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,有时前后质量看似不相等,是由于反应前有气体参加,或反应后有气体生成没有加进去,这题反应前氯酸钾和二氧化锰的质量为17.0g,而反应后剩余固体质量只有12.2g,分析原因,因为反应生成了氧气。所以很快可以算出反应生成氧气的质量17.0g-12.2g=4.8g,再根据化学放应方程式2KClO3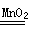 2KCl + 3O2 ↑中氯酸钾,氯化钾与氧气的质量关系,算出氯酸钾或氯化钾均可
2KCl + 3O2 ↑中氯酸钾,氯化钾与氧气的质量关系,算出氯酸钾或氯化钾均可
解:设12.2g剩余的混合物中含有氯化钾的质量为x。
设12.2g剩余的混合物中含有氯化钾的质量为x。
2KClO3 2KCl + 3O2↑
2KCl + 3O2↑
149 96
x 4.8g 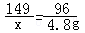
x=7.45g
12.2g - 7.45g = 4.75g
答:剩余的混合物中二氧化锰的质量为4.75g
考点:根据化学方程式计算

练习册系列答案
相关题目
下图是胃得乐牌胃药的部分标识。胃药中所含的物质能中和胃里过多的胃酸(主要是盐酸)。某患者按标识上的服用方法服药三天后病情好转。计算患者在三天内所服用的此胃药中(计算结果取整数):
| 胃得乐牌 功能:主治胃酸过多引起的胃病 成分:每片含氢氧化镁250 mg 服用方法:每日三次,每次2片 |
(1)所含氢氧化镁的质量为____________ mg。
(2)理论上可中和胃酸中的HCl的质量为____________ mg。

