题目内容
【题目】铜能与硝酸溶液反应,且浓度不同,产物不同。现将一定质量的铜逐渐加入144g浓硝酸中,反应生成的气体质量随铜的质量变化关系如图所示。
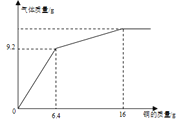
已知:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)硝酸铜中,铜、氮、氧三种元素的质量比为___________。
(2)反应过程中生成的NO的质量为___________________。
(3)当硝酸浓度过低时,反应基本停止。经测定,实验结束后得到的混合溶液中溶质HNO3的质量为25.2g,求原浓硝酸溶液的溶质质量分数________。(写出计算过程,结果0.1%)
【答案】16:7:24; 3g 52.5%
【解析】
(1)硝酸铜中,铜、氮、氧三种元素的质量比为64:14×2:16×6=16:7:24;
(2)设生成一氧化氮的质量为x,反应的硝酸的质量为y
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
192 504 60
9.6g y x
![]() x=3g
x=3g
![]() y=25.2g
y=25.2g
(3)设与6.4g 铜反应的浓硝酸的质量为m
Cu+ 4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
64 252
6.4g m
![]() m=25.2g
m=25.2g
当硝酸浓度过低时,反应基本停止。经测定,实验结束后得到的混合溶液中溶质HNO3的质量为25.2g,原浓硝酸溶液的溶质质量分数
![]()

练习册系列答案
相关题目