��Ŀ����
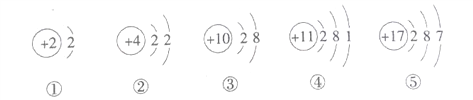
����Ŀ����ѧ�����Ƴ�һ����Ԫ���ȵ�ԭ�����Ӱڵ��ӣ����������ȷ���ӡ���ͼA����Ԫ����Ԫ�����ڱ��е������Ϣ����ͼB����Ԫ���γɵ�һ�����ӵĽṹʾ��ͼ��

��1����Ԫ�ص����ԭ������Ϊ___________ ��
��2��ͼB�е�x =_____�������ӵķ����� ____________ ��
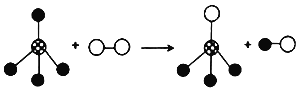
��3����ͼ��ʾ������Sr��ѧ�������Ƶ���_______ ������ţ�
��4����Ԫ����Sr��ѧ����Ҳ���ƣ���Ca(OH)2�и�Ԫ�صĻ��ϼ�Ϊ______��Ca(OH)2��������ж�����̼��Ӧ���仯ѧ����ʽΪ��____________________ ��
��Ԫ�ص������ﻯѧʽΪ___________ ��
���𰸡� 87.62 38 Sr2+ �� +2 CO2 + Ca(OH)2 == CaCO3 ��+ H2O SrO
��������(1)��Ԫ�����ڱ�����Ϣ��֪����Ԫ�ص����ԭ������Ϊ87.62��(2)��Ϊԭ������=�˵����������X=38��ͼ2�к��������Ϊ2+8+18+8=36��ʧȥ���������ӣ���2����λ������ɣ�����Ϊ��Sr2+��(3)Srԭ����ʧȥ2�����ӣ�Aֻ��һ�����Ӳ㣬�õ��Ӳ�����2�����ӣ������ȶ��ṹ������������������ӣ���ʧȥ�������ӣ���ѧ������Sr���ƣ� Ca(OH)2��OH�Ļ��ϼ�Ϊ-1�����Ԫ�صĻ��ϼ�Ϊ+2��Ca(OH)2��������ж�����̼��Ӧ���仯ѧ����ʽΪ��CO2+Ca(OH)2=CaCO3��+H2O��Srԭ����ʧȥ2����������2����λ������ɣ�������Ԫ�ص������ﻯѧʽΪ��SrO��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ����100gˮ�в��ϼ������A��ı��¶ȣ��õ���Ӧ����Һ��~�ݡ�����˵����ȷ����( )
![]()
���ϣ�A���ܽ�� | |||||
�¶�/�� | 20 | 30 | 40 | 50 | 60 |
�ܽ��/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
A. ����A������������� B. �ۢ���A�������������
C. �ڢܢݵ���ҺΪ������Һ D. �٢ۢܢ���û�й������
����Ŀ������ͭ����ͭ��п�Ͻ�Ϊ�˲ⶨij��ͭ��Ʒ��ͭ�������������ס��ҡ�����λͬѧ�ֱ����ʵ�飬ʵ���������£����ձ�����Ϊ56 g��
�� | �� | �� | |
���ձ�+ϡ���ᣩ���� | 139 g | 129 g | 129 g |
�����ͭ��Ʒ���� | 20 g | 24 g | 20 g |
��ַ�Ӧ���ձ�+ʣ�����ʣ����� | 158.8 g | 152.8 g | 148.8 g |
��1��ʵ��֤����λͬѧ�У�ֻ��һλͬѧȡ�õ�ϡ�������Ʒǡ����ȫ��Ӧ�����ͬѧ����λͬѧ��
��2������㣺��ͭ��Ʒ��ͭ������������Zn + 2HCl ===== Zn Cl2 + H2��