题目内容
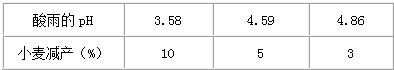
16、酸雨是指pH<5.6的雨、雪等各种形式的大气降水.它主要是由含硫燃料(煤和石油)燃烧和金属冶炼厂释放的二氧化硫气体造成的.酸雨的危害极大,减少二氧化硫等污染物的排放对保护环境是非常重要的.某校化学兴趣小组同学,取刚降到地面的酸雨水样,每隔一定时间测定其pH,数据如下:
(1)由测定的数据可知,在测定的4分钟内的酸雨水样的酸性 增强(选填“减弱”或“增强”);
(2)在测定的时间内,酸雨水样pH发生变化的主要原因是酸雨中的亚硫酸(化学式是
H2SO3)被空气中的氧气氧化为硫酸的缘故.请写出反应的化学方程式:H2SO3+O2═H2SO4.

(1)由测定的数据可知,在测定的4分钟内的酸雨水样的酸性 增强(选填“减弱”或“增强”);
(2)在测定的时间内,酸雨水样pH发生变化的主要原因是酸雨中的亚硫酸(化学式是
H2SO3)被空气中的氧气氧化为硫酸的缘故.请写出反应的化学方程式:H2SO3+O2═H2SO4.
分析:根据溶液PH的变化情况判断溶液酸碱性变化趋势.硫酸比亚硫酸更容易电离,所以酸性逐渐增强.按书写化学方程式的方法正确书写化学方程式.
解答:解:(1)溶液的PH越来越小,酸性越来越强.
故填:增强
(2)化学方程式为:H2SO3+O2═H2SO4.
故填:增强
(2)化学方程式为:H2SO3+O2═H2SO4.
点评:本题主要考查了溶液的PH与溶液酸碱性的关系以及如何正确书写化学方程式的内容.

练习册系列答案
相关题目