题目内容
【题目】向一块部分被氧化的铝片中加入稀盐酸至恰好完全反应,生成氢气0.2 g,反应后将所得溶液蒸干得到氯化铝13.35 g。计算:
(1)铝反应消耗的盐酸溶质的质量。
(2)氧化铝反应消耗的盐酸溶质的质量。
【答案】(1)7.3g;(2)3.65g。
【解析】
由题意铝与稀盐酸反应生成氯化铝和氢气,氧化铝和稀盐酸反应生成氯化铝和水,
设铝反应消耗的盐酸溶质的质量为![]() ,铝反应生成的氯化铝的质量为
,铝反应生成的氯化铝的质量为![]() ,则有:
,则有:

由![]() 解得
解得![]()
由![]() 解得
解得![]()
(1)铝反应消耗的盐酸溶质的质量为7.3g;
(2)氧化铝和稀盐酸反应生成的氯化铝和水,生成氯化铝的质量为13.35g-8.9g=4.45g,根据质量守恒定律元素守恒可知氯化铝中氯元素全部来自于稀盐酸中的氯化氢,设参加反应的氯化氢的质量为![]() ,根据氯元素守恒则有:
,根据氯元素守恒则有:
![]()
解得![]()
则氧化铝反应消耗的盐酸溶质的质量为3.65g
答:(1)铝反应消耗的盐酸溶质的质量为7.3g;
(2)氧化铝反应消耗的盐酸溶质的质量是3.65g。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
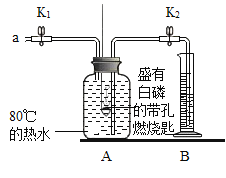
【题目】用下图所示装置研究燃烧条件和测定空气中氧气含量实验。
已知:白磷的着火点为40℃。
实验装置 | 实验步骤和现象 |
| 步骤Ⅰ:检查装置气密性,气密性良好。 步骤Ⅱ:将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧 步骤Ⅲ:向A瓶中加满80℃的热水,塞紧瓶塞,白磷不燃烧。 步骤Ⅳ:打开K1和K2, 从a口向瓶中鼓入空气,待瓶中液面低于燃烧匙底部时,关闭K1和K2此时进入量筒B中水的体积为200ml,观察到A瓶中白磷燃烧。 |
(1)对比步骤Ⅱ和Ⅳ的现象可知,可燃物的燃烧条件之一是_____。
(2)待装置冷却至室温后,打开K2,可观察到量筒中液面的刻度为___,说明空气中氧气的体积约占1/5。