题目内容
(2011?朝阳区二模)工业上制备铝的化学方程式为 2Al2O3═4Al+3O2↑,则由102g氧化铝制得铝的质量是多少?
【答案】分析:根据氧化铝分解生成铝和氧气反应的化学方程式,可得知反应中氧化铝与生成金属铝间的质量关系,根据这种质量关系,可由氧化铝的质量计算制得铝的质量.
解答:解:设制得铝的质量是x
2Al2O3═4Al+3O2↑
204 108
102g x
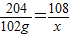
x=54g
答:由102g氧化铝制得铝的质量为54g.
点评:利用反应的化学方程式,可计算出反应中各物质的质量关系,根据物质的质量关系可由已知物质的质量计算其它物质的质量.
解答:解:设制得铝的质量是x
2Al2O3═4Al+3O2↑
204 108
102g x
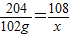
x=54g
答:由102g氧化铝制得铝的质量为54g.
点评:利用反应的化学方程式,可计算出反应中各物质的质量关系,根据物质的质量关系可由已知物质的质量计算其它物质的质量.

练习册系列答案
相关题目
(2011?朝阳区二模)某化学活动小组用稀盐酸对赤铁矿中Fe2O3含量进行测定(杂质不与盐酸反应且不溶于水),得到一黄色残液.为防止直接排放造成环境污染,对其进行了处理,过滤该残液,取100g 滤液,向其中不断加入某未知溶质质量分数的氢氧化钠溶液,所得
实验数据如下表:
(资料:FeCl3+3NaOH=Fe(OH)3↓+3NaCl)
通过对上述实验数据的分析,选择合理的数据,计算所加氢氧化钠溶液中溶质的质量分数.
实验数据如下表:
| 加入氢氧化钠溶液的总质量/g | 20 | 40 | 60 | 80 | 140 | 160 |
| 生成沉淀的质量/g | 1.07 | 2.14 | 5.35 | 5.35 |
通过对上述实验数据的分析,选择合理的数据,计算所加氢氧化钠溶液中溶质的质量分数.